共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問32 (化学基礎(第2問) 問1(3))
問題文
アボガドロは、気体の種類によらず、同温・同圧で同体積の気体には、同数の分子が含まれるという仮説を提唱した。この仮説は、今日ではアボガドロの法則として知られている。次の実験Ⅰは、アボガドロの法則に基づいて、貴ガス(希ガス)元素の一つであるクリプトンKrの原子量を求めることを目的としたものである。
実験Ⅰ
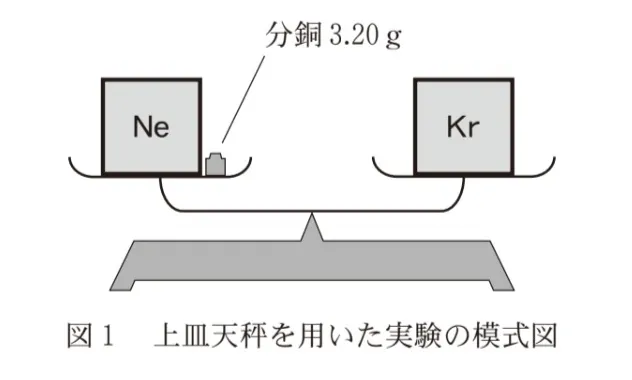
ネオンNe 1.00gが入った容器がある。大きさと質量が等しい別の容器に、同温・同圧で同じ体積のKrを入れ、両方の容器を上皿天秤(びん)にのせた。両方の皿がつり合うには、図1に示すように、Neが入った容器をのせた皿に3.20gの分銅が必要であった。
NeとKrの原子は、いずれも最外殻電子の数が( ア )個である。これらの原子は、他の原子と反応したり結合をつくったりしにくい。このため、価電子の数は( イ )個とみなされる。NeとKrはいずれも単原子分子として存在するので、Neの原子量が20であることを用いて、Krの原子量を求めることができる。
b 実験Ⅰで用いたKrは、0℃、1.013✕105Paで何Lか。最も適当な数値を、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問32(化学基礎(第2問) 問1(3)) (訂正依頼・報告はこちら)
アボガドロは、気体の種類によらず、同温・同圧で同体積の気体には、同数の分子が含まれるという仮説を提唱した。この仮説は、今日ではアボガドロの法則として知られている。次の実験Ⅰは、アボガドロの法則に基づいて、貴ガス(希ガス)元素の一つであるクリプトンKrの原子量を求めることを目的としたものである。
実験Ⅰ
ネオンNe 1.00gが入った容器がある。大きさと質量が等しい別の容器に、同温・同圧で同じ体積のKrを入れ、両方の容器を上皿天秤(びん)にのせた。両方の皿がつり合うには、図1に示すように、Neが入った容器をのせた皿に3.20gの分銅が必要であった。
NeとKrの原子は、いずれも最外殻電子の数が( ア )個である。これらの原子は、他の原子と反応したり結合をつくったりしにくい。このため、価電子の数は( イ )個とみなされる。NeとKrはいずれも単原子分子として存在するので、Neの原子量が20であることを用いて、Krの原子量を求めることができる。
b 実験Ⅰで用いたKrは、0℃、1.013✕105Paで何Lか。最も適当な数値を、次の選択肢のうちから一つ選べ。

- 0.560L
- 1.12L
- 1.68L
- 2.24L
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
この問題で覚えておくことは、すべての気体は標準状態で1mol=22.4Lであることです。
Ne1gの物質量は標準状態で 1÷20=0.05molです。
同温同圧で同体積であることからKrも0.05molの物質量であり、全ての気体は1mol=22.4Lであることから、
22.4×0.05=1.12Lとなります。
参考になった数0
この解説の修正を提案する
02
この問題のポイントは標準状態(0℃、1.013×10⁵Pa)において、気体は1molあたり22.4Lの体積を占めるということを覚えているかどうかにあります。
まず実験Ⅰで用いられたNeの物質量は、Neの原子量が20なので
1.00g/20g/mol=5.0×10⁻²mol
となります。
実験Ⅰで用いたNeとKrは同温・同圧で同じ体積なので同数の分子、つまり同じ物質量の分子が含まれていることになります。
したがって、実験Ⅰで用いたKrの0℃、1.013×10⁵Paにおける体積は
22.4L/mol✕5.0×10⁻²mol=1.12L
と求めることができます。
参考になった数0
この解説の修正を提案する
03
まずはじめに、Krの原子量を求めます。
Neの原子量:Krの原子量=Neの質量:Krの質量
Neの原子量およびNeとKrの質量が分かっているので、以下のように求まります。
20:Krの質量=1.00g:4.20g
Krの原子量=4.20×20 =84.0g/mol
次にKrの物質量を求めます。
Krの物質量=4.20g×84.0g/mol =0.050mol
Krは0℃、1.013✕105Paの標準状態であるので、1molあたりの気体の体積は22.4Lです。
したがって、Krの体積は、以下のように求まります。
0.050mol×22.4L/mol=1.12L
0℃、1.013✕105Paの標準状態では、1molあたりの気体の体積は22.4Lであることを覚えておきましょう!
参考になった数0
この解説の修正を提案する
前の問題(問31)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問33)へ