共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問35 (化学基礎(第2問) 問2(1))
問題文
プルーストは、一つの化合物を構成している成分元素の質量の比は、常に一定であるという定比例の法則を提唱した。次の実験Ⅱは、炭酸ストロンチウムSrCO3を強熱すると、次の式(1)に示すように、固体の酸化ストロンチウムSrOと二酸化炭素CO2に分解することを利用して、ストロンチウムSrの原子量を求めることを目的としたものである。
SrCO3→SrO+CO2 (1)
実験Ⅱ
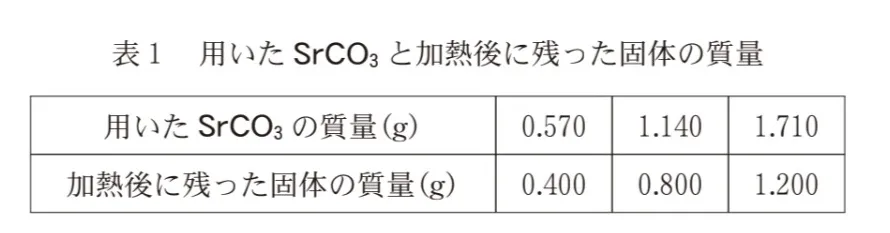
細かくすりつぶしたSrCO3をはかりとり、十分な時間強熱した。用いたSrCO3の質量と加熱後に残った固体の質量との関係は、表1のようになった。
式(1)の反応では、分解するSrCO3と生じるSrOの質量の( ウ )は、発生するCO2の質量に等しい。
また、生じるSrOとCO2の質量の( エ )は、分解するSrCO3の量にかかわらず一定となる。したがって、炭素Cと酸素Oの原子量を用いて、Srの原子量を求めることができる。
a 空欄( ウ )・( エ )に当てはまる語の組合せとして最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問35(化学基礎(第2問) 問2(1)) (訂正依頼・報告はこちら)
プルーストは、一つの化合物を構成している成分元素の質量の比は、常に一定であるという定比例の法則を提唱した。次の実験Ⅱは、炭酸ストロンチウムSrCO3を強熱すると、次の式(1)に示すように、固体の酸化ストロンチウムSrOと二酸化炭素CO2に分解することを利用して、ストロンチウムSrの原子量を求めることを目的としたものである。
SrCO3→SrO+CO2 (1)
実験Ⅱ
細かくすりつぶしたSrCO3をはかりとり、十分な時間強熱した。用いたSrCO3の質量と加熱後に残った固体の質量との関係は、表1のようになった。
式(1)の反応では、分解するSrCO3と生じるSrOの質量の( ウ )は、発生するCO2の質量に等しい。
また、生じるSrOとCO2の質量の( エ )は、分解するSrCO3の量にかかわらず一定となる。したがって、炭素Cと酸素Oの原子量を用いて、Srの原子量を求めることができる。
a 空欄( ウ )・( エ )に当てはまる語の組合せとして最も適当なものを、次の選択肢のうちから一つ選べ。

- ウ:和 エ:和
- ウ:和 エ:差
- ウ:和 エ:比
- ウ:差 エ:和
- ウ:差 エ:差
- ウ:差 エ:比
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
定比例の法則は、「化合物を構成する元素の質量比は常に一定である」というものです。
つまり、1molのSrCO3からは、1molのSrOと1molのCO2が生成します。
SrOの分子量をA、CO2のBとすると
SrCO3の分子量Cは、C=A+Bで表されます。
回答では、C-A=B で差となります。
SrCO3の物質量をnとすると、
nC=nA+nBであり、
生じるSrOの質量=nA、生じるCO2の質量=nBとなり、
回答では、nA/nBは常に一定となります。答えは比です。
参考になった数0
この解説の修正を提案する
02
まず式⑴に注目してみると、SrCO₃が分解してSrOとCO₂のみが生じていることが分かります。
このことから、分解するSrCO₃と生じるSrOの質量の差が、発生するCO₂の質量に等しいということになります。
また、生じるSrOとCO₂の物質量を見てみると、常に1:1と一定であることも式⑴より読み取れるので、その質量の比は分解するSrCO₃の量にかかわらず一定となるといえます。
以上のことから、空欄ウ・エに当てはまる語の組合せとして最も適当であるのは差・比ということが分かります。
参考になった数0
この解説の修正を提案する
03
(ウ)
反応前と反応後の質量は等しいです。
つまり、
SrCO3の質量=SrOの質量+CO2の質量
CO2の質量=SrCO3の質量−SrOの質量
となります。したがって、答えは“差”です。
(エ)
問題文にもあるように、“プルーストは、一つの化合物を構成している成分元素の質量の比は、常に一定であるという定比例の法則を提唱”しました。
つまり、SrCO3から一定のSrOとCO2が生じます。
したがって、答えは“比”です。
参考になった数0
この解説の修正を提案する
前の問題(問33)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問36)へ