共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問24 (化学基礎(第1問) 問8(b))
問題文
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
二枚貝の貝殻は、炭酸カルシウムCaCO3(式量100)を主成分として含んでいる。CaCO3は塩酸と反応して二酸化炭素CO2を発生する。このときの反応は次の式(3)で表される。
CaCO3+2HCl → CaCl2+H2O+CO2 (3)
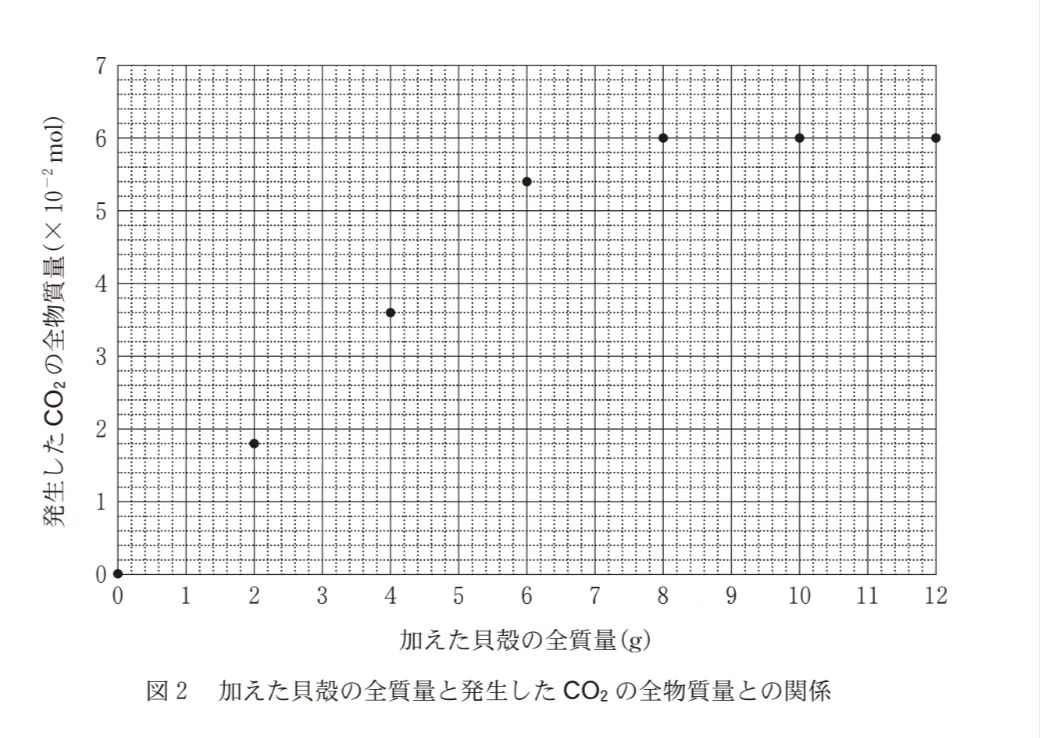
貝殻に含まれるCaCO3の含有率(質量パーセント)を知る目的で、濃度c(mol/L)の塩酸50mLに貝殻の粉末を2.0gずつ加えて十分に反応させ、発生したCO2の物質量を調べた。図2は実験結果をまとめたものである。後の問いに答えよ。ただし、貝殻に含まれるCaCO3以外の成分は塩酸とは反応せず、発生したCO2の水溶液への溶解は無視できるものとする。
この実験で用いた貝殻に含まれるCaCO3の含有率(質量パーセント)は何%か。最も適当な数値を、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問24(化学基礎(第1問) 問8(b)) (訂正依頼・報告はこちら)
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
二枚貝の貝殻は、炭酸カルシウムCaCO3(式量100)を主成分として含んでいる。CaCO3は塩酸と反応して二酸化炭素CO2を発生する。このときの反応は次の式(3)で表される。
CaCO3+2HCl → CaCl2+H2O+CO2 (3)
貝殻に含まれるCaCO3の含有率(質量パーセント)を知る目的で、濃度c(mol/L)の塩酸50mLに貝殻の粉末を2.0gずつ加えて十分に反応させ、発生したCO2の物質量を調べた。図2は実験結果をまとめたものである。後の問いに答えよ。ただし、貝殻に含まれるCaCO3以外の成分は塩酸とは反応せず、発生したCO2の水溶液への溶解は無視できるものとする。
この実験で用いた貝殻に含まれるCaCO3の含有率(質量パーセント)は何%か。最も適当な数値を、次の選択肢のうちから一つ選べ。

- 40
- 45
- 80
- 86
- 90
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
図2より、貝殻を 2.0 g加えたとき、発生した CO₂ の物質量は1.8 × 10-2 molです。
このとき、塩酸は十分であり、貝殻中の CaCO₃ がすべて反応していると考えられます。
反応式より、CaCO₃ 1 molから CO₂ 1 molが発生します。
したがって、貝殻 2.0 g中に含まれる CaCO₃ の物質量は1.8 × 10-2 mol です。
CaCO₃ の式量は 100 なので、質量は1.8 × 10-2 mol × 100 g/mol = 1.8 gです。
したがって、貝殻中の CaCO₃ の含有率は(1.8 g ÷ 2.0 g)× 100 = 90% となります。
参考になった数0
この解説の修正を提案する
02
CaCO3が完全に反応した時のCaCO3の物質量と貝殻の重量が分かれば
貝殻に含まれるCaCO3の含有率を求めることができます。
CO2量が頭打ちになるまでのグラフは1次関数になっています。
加えた貝殻の量をx、CO2の物質量をyとすると
y=0.009xのグラフであると読み取れます。
yが最大量の6×10-2molのとき、xは約6.7gです。
貝殻6.7gからCO2が6×10-2mol発生したことになります。
(3)の式より、1molのCO2が発生するとき、CaCO3は1mol反応します。
よって、貝殻6.7gにはCaCO3が6×10-2mol含まれていると分かります。
CaCO3の式量は100のため
CaCO3の重量は100g/mol×6×10-2mol=6gです。
貝殻に含まれるCaCO3の含有率は、6g/6.7g×100≒90%です。
参考になった数0
この解説の修正を提案する
前の問題(問23)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問25)へ