共通テスト(理科) 過去問
令和6年度(2024年度)本試験
問95 (化学(第2問) 問4)
問題文
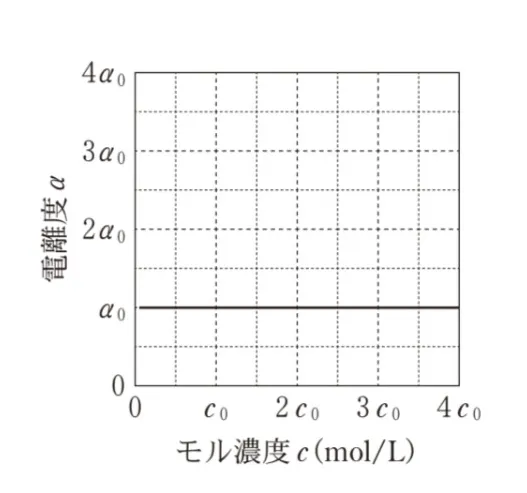
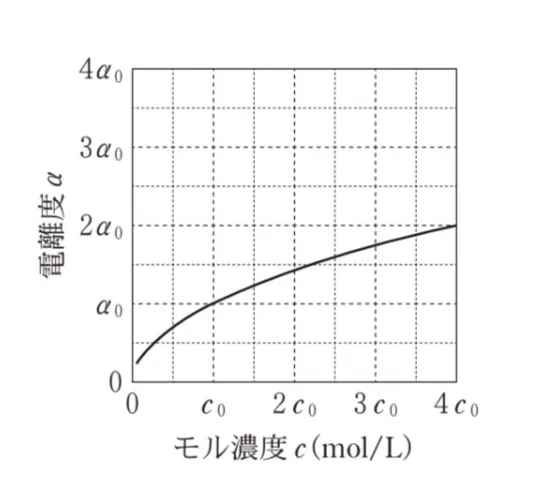
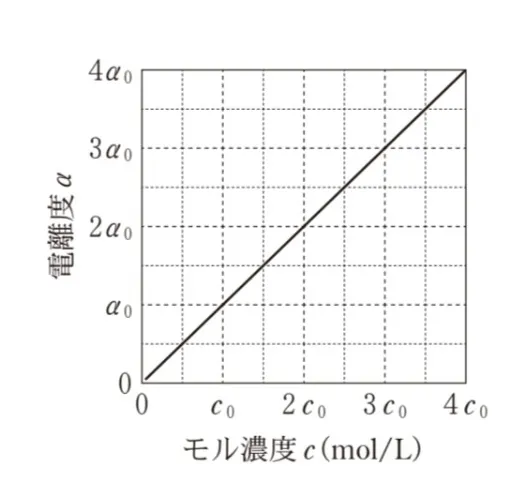
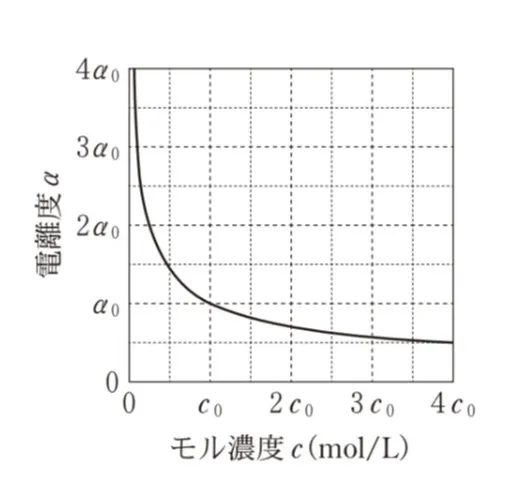
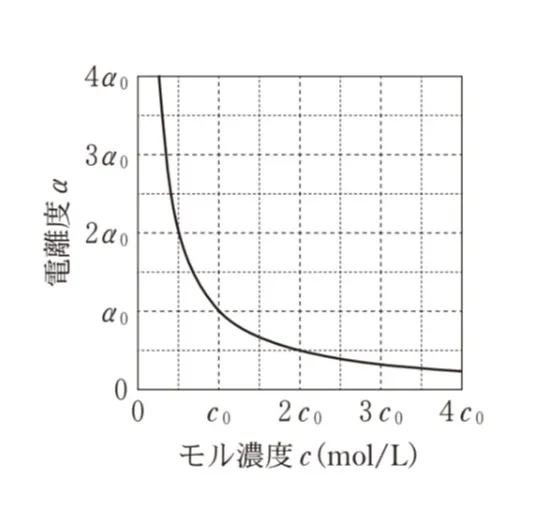
純水に弱酸HAを溶解させた水溶液を考える。HA水溶液のモル濃度c(mol/L)とHAの電離度αの関係を表したグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。ただし、HA水溶液のモル濃度がc0(mol/L)のときのHAの電離度をα0とし、αは1よりも十分小さいものとする。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和6年度(2024年度)本試験 問95(化学(第2問) 問4) (訂正依頼・報告はこちら)
純水に弱酸HAを溶解させた水溶液を考える。HA水溶液のモル濃度c(mol/L)とHAの電離度αの関係を表したグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。ただし、HA水溶液のモル濃度がc0(mol/L)のときのHAの電離度をα0とし、αは1よりも十分小さいものとする。
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
弱酸の電離度αとモル濃度cの関係を問う問題です。
弱酸HAの電離平衡はHA ⇌ H+ + A-で表され、電離定数Kaは次のように表されます。
Ka = c×α2 / (1-α)
αは1より十分小さいので(1-α)≈1とすると
Ka = c×α2
よってα = √(Ka/c)
cが大きくなるほどαは小さくなります。またαはcの平方根に反比例するため、単純な反比例より緩やかに減少する曲線になります。
この選択肢が正解です。
参考になった数0
この解説の修正を提案する
02
電離度とモル濃度のグラフで最も適当なグラフを選びます。
H+,A-,HAそれぞれのモル濃度の変化量は、
H+:cα A-:cα HA:c(1-α)となります。
HAは弱酸であるため電離定数をKとすると、
K=[H+][A-]/[HA]=(cα)(cα)/c(1-α)=cα2/1-α
αが1よりも十分小さいことより、
K=cα2
よってcとαが反比例のグラフを選べばよい。
この選択肢が正解になります。
これはK=cαのグラフです。
数値を当てはめて確認をすることができます。
参考になった数0
この解説の修正を提案する
03
濃度が小さくなるほど電離度は大きくなります。
弱酸HAの電離は HA⇔H++A-
電離定数K=([H+]+[A-])/[HA]
[H+]=cα
[A-]=cα
[HA]=c(1-α)≒cとなる。
K=cα×cα/c=cα2より、
α=√K/c
であり、Kは定数であるため
α∝√1/cとなる。
これと図を見比べるとよいでしょう。
濃度を4倍にすると
電離度は√(1/4)=1/2になります。
参考になった数0
この解説の修正を提案する
前の問題(問94)へ
令和6年度(2024年度)本試験 問題一覧
次の問題(問96)へ