共通テスト(理科) 過去問
令和6年度(2024年度)本試験
問96 (化学(第2問) 問5)
問題文
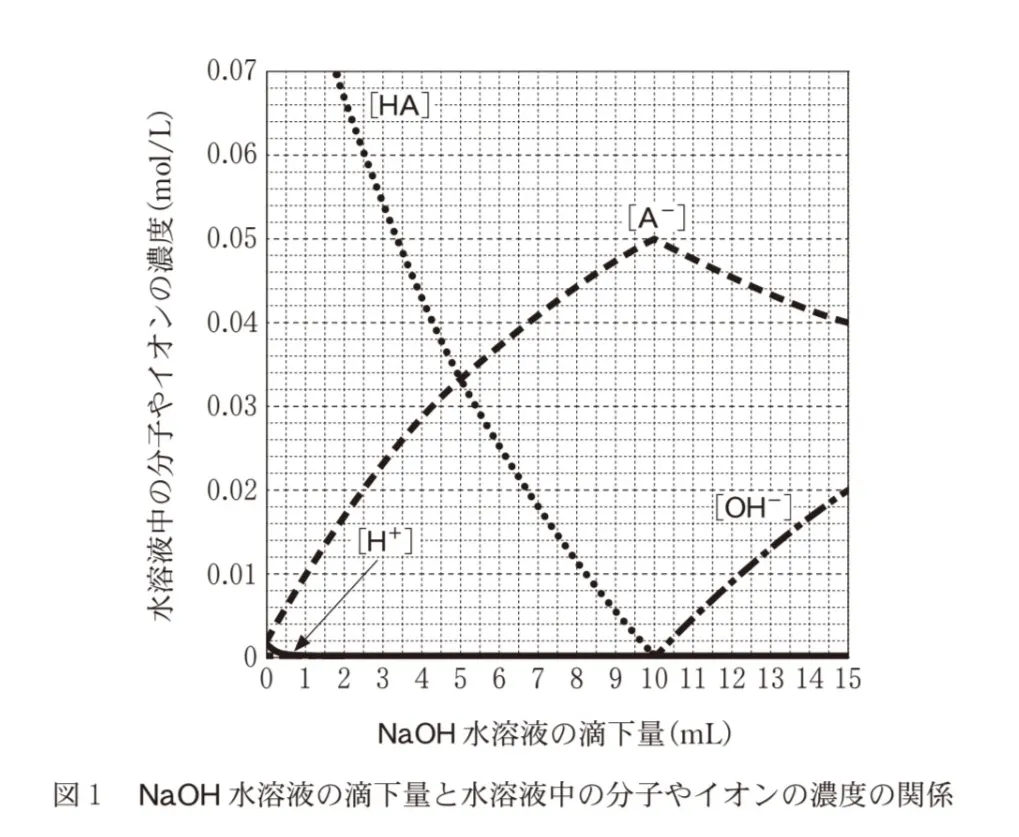
モル濃度0.10mol/LのHA水溶液10.0mLに、モル濃度0.10mol/LのNaOH水溶液を滴下すると、水溶液中のHA、H+、A−、OH−のモル濃度[HA]、[H+]、[A−]、[OH−]は、図1のように変化する。NaOH水溶液の滴下量が2.5mLのとき、H+のモル濃度は[H+]=8.1✕10−5mol/Lである。弱酸HAの電離定数Kaは何mol/Lか。最も適当な数値を、後の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和6年度(2024年度)本試験 問96(化学(第2問) 問5) (訂正依頼・報告はこちら)
モル濃度0.10mol/LのHA水溶液10.0mLに、モル濃度0.10mol/LのNaOH水溶液を滴下すると、水溶液中のHA、H+、A−、OH−のモル濃度[HA]、[H+]、[A−]、[OH−]は、図1のように変化する。NaOH水溶液の滴下量が2.5mLのとき、H+のモル濃度は[H+]=8.1✕10−5mol/Lである。弱酸HAの電離定数Kaは何mol/Lか。最も適当な数値を、後の選択肢のうちから一つ選べ。

- 2.0✕10−5mol/L
- 2.7✕10−5mol/L
- 1.1✕10−4mol/L
- 2.4✕10−4mol/L
- 3.2✕10−4mol/L
- 6.7✕10−3mol/L
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
電離定数KaをKa = [H+][A-]/[HA]の式から求める問題です。NaOH2.5mL滴下時の[HA]と[A-]を計算で求め、与えられた[H+]を代入します。
NaOH2.5mL滴下時の各濃度を求めます。
HAの初期物質量は0.10mol/L×10.0mL=1.0mmol
加えたNaOHは0.10mol/L×2.5mL=0.25mmol
NaOHはHAと1:1で反応するので、反応後のHA=0.75mmol、A-=0.25mmolとなります。
総体積は12.5mLなので
[HA] = 0.75/12.5 = 0.060mol/L [A-] = 0.25/12.5 = 0.020mol/L
Ka = [H+][A-]/[HA] = 8.1×10-5 × 0.020/0.060 = 2.7×10-5 mol/L
この選択肢が正解です。
参考になった数0
この解説の修正を提案する
02
電離平衡の式Ka=[H+][A-]/[HA]を使って求めるため、
それぞれの濃度を求めます。
HAの濃度は
0.1×0.01=1.0×10-3mol
NaOHの物質量は
0.1×2.5×10-3=2.5×10-4mol
HAの残りの物質量は
(1.0×10-3)ー(2.5×10-4)=7.5×10-4mol
また、A-の物質量は2.5×10-4 mol
上記の式に代入すると
Ka=[H+][A-]/[HA]=(8.1✕10−5mol/L)(2.5×10-4 mol)/7.5×10-4mol
=2.7×10-5mol/Lとなります。
この選択肢が正解になります。
電離平衡の式ですが、単位に注目することで、間違いに気づくこともあります。
参考になった数0
この解説の修正を提案する
03
緩衝溶液の式を用います。
HAの濃度は0.1×0.01=1.0×10-3molです。
加えたNaOHは0.1×0.0025=2.5×10-4molです。
中和されずに残ったHAは
1.0×10-3ー2.5×10-4=7.5×10-4mol
生成するA-は2.5×10-4 molです。
よって、
[A-]/[HA]=2.5×10-4 /7.5×10-4=1/3です。
電離平衡の式より、
Ka=[H+][A-]/[HA]より、
Ka=[H+]/3=2.7✕10−5となります。
参考になった数0
この解説の修正を提案する
前の問題(問95)へ
令和6年度(2024年度)本試験 問題一覧
次の問題(問97)へ