共通テスト(理科) 過去問
令和7年度(2025年度)追・再試験
問101 (化学(第2問) 問6)
問題文
原料であるボーキサイトは、Al2O3・nH2Oを主成分とし、SIO2やFe2O3を含むので、Al2O3を取り出す必要がある。
ボーキサイトの粉末を、加熱した高濃度の水酸化ナトリウムNaOH水溶液に混ぜると、溶解しない化合物と、テトラヒドロキシドアルミン酸イオン[Al(OH)4]−を含む溶液に分離できる。(a)[Al(OH)4]−を含む溶液に二酸化炭素CO2の気体を通じると、(b)水酸化アルミニウムAl(OH)3の沈殿が生じる。沈殿として取り出した(c)Al(OH)3を加熱することでAl2O3が得られる。
得られた(d)Al2O3を氷晶石Na3AlF6とともに約1000℃で融解させ、溶融塩(融解塩)電解することで、Alを得ることができる。
c 溶融塩電解で得たAlを原料としてつくられる硫酸アンモニウムアルミニウム十二水和物Al(NH4)(SO4)2・12H2O(式量453)は、再結晶を繰り返すことで高純度の結晶になる。この結晶を加熱すると、脱水が起こり300℃までにはAl(NH4)(SO4)2(式量237)に変化する。そのまま加熱すると約450℃から変化が起こり、約550℃までにはAl2(SO4)3(式量342)となる。引き続いて加熱すると約650℃からさらに変化が起こり、950℃に達すると高純度のAl2O3(式量102)が得られる。これはファインセラミックスなどに用いられる。
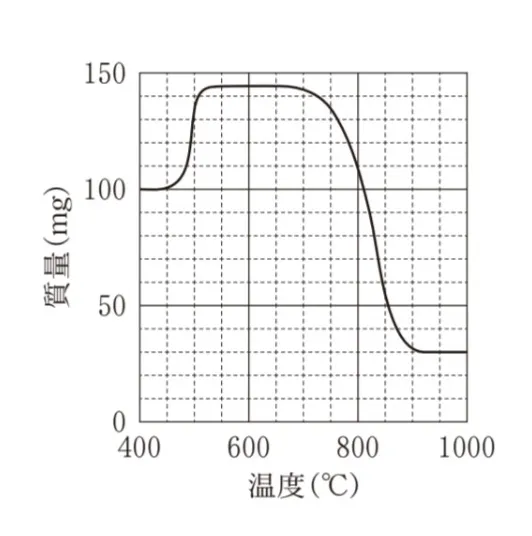
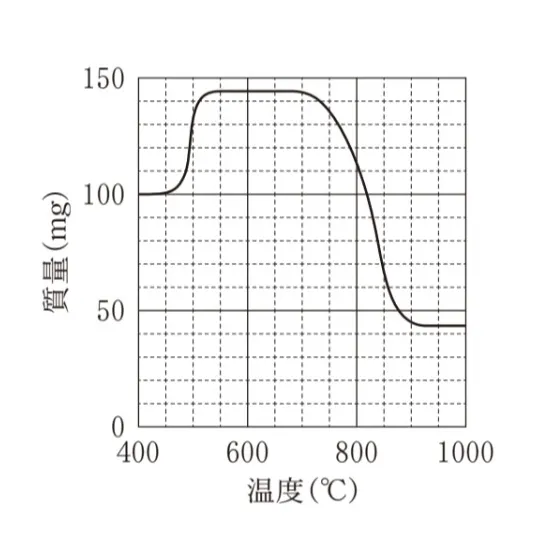
100mgのAl(NH4)(SO4)2を400℃から1000℃まで加熱したときの温度と質量の関係を表すグラフとして最も適当なものを、次のうちから一つ選べ。ただし、Al(NH4)(SO4)2のアルミニウムはすべてAl2O3になるものとする。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和7年度(2025年度)追・再試験 問101(化学(第2問) 問6) (訂正依頼・報告はこちら)
原料であるボーキサイトは、Al2O3・nH2Oを主成分とし、SIO2やFe2O3を含むので、Al2O3を取り出す必要がある。
ボーキサイトの粉末を、加熱した高濃度の水酸化ナトリウムNaOH水溶液に混ぜると、溶解しない化合物と、テトラヒドロキシドアルミン酸イオン[Al(OH)4]−を含む溶液に分離できる。(a)[Al(OH)4]−を含む溶液に二酸化炭素CO2の気体を通じると、(b)水酸化アルミニウムAl(OH)3の沈殿が生じる。沈殿として取り出した(c)Al(OH)3を加熱することでAl2O3が得られる。
得られた(d)Al2O3を氷晶石Na3AlF6とともに約1000℃で融解させ、溶融塩(融解塩)電解することで、Alを得ることができる。
c 溶融塩電解で得たAlを原料としてつくられる硫酸アンモニウムアルミニウム十二水和物Al(NH4)(SO4)2・12H2O(式量453)は、再結晶を繰り返すことで高純度の結晶になる。この結晶を加熱すると、脱水が起こり300℃までにはAl(NH4)(SO4)2(式量237)に変化する。そのまま加熱すると約450℃から変化が起こり、約550℃までにはAl2(SO4)3(式量342)となる。引き続いて加熱すると約650℃からさらに変化が起こり、950℃に達すると高純度のAl2O3(式量102)が得られる。これはファインセラミックスなどに用いられる。
100mgのAl(NH4)(SO4)2を400℃から1000℃まで加熱したときの温度と質量の関係を表すグラフとして最も適当なものを、次のうちから一つ選べ。ただし、Al(NH4)(SO4)2のアルミニウムはすべてAl2O3になるものとする。
正解!素晴らしいです
残念...

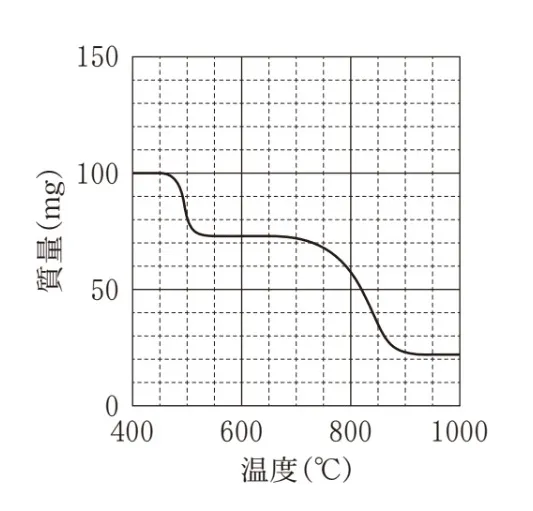
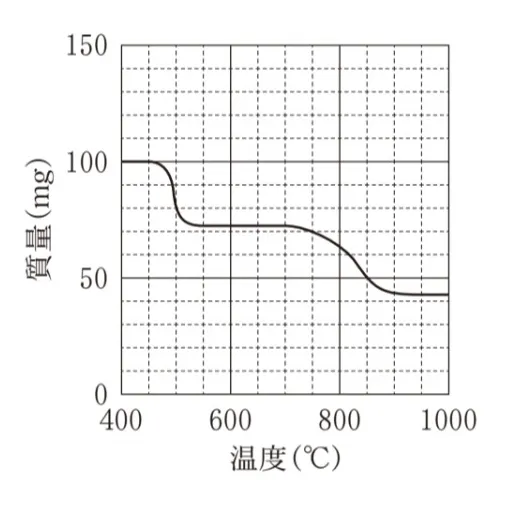
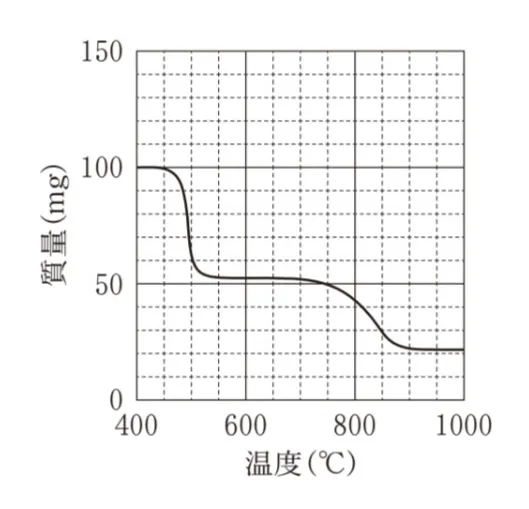
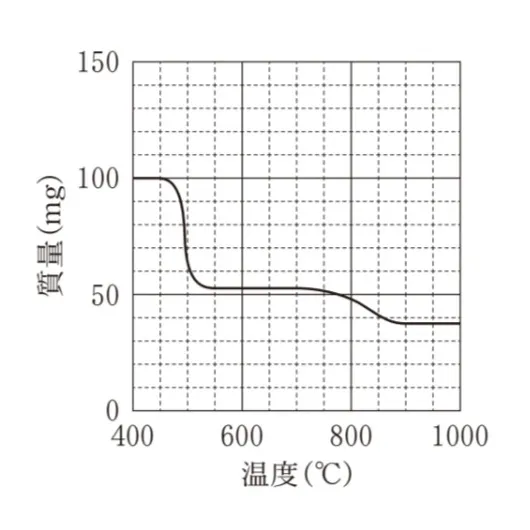
この過去問の解説
前の問題(問100)へ
令和7年度(2025年度)追・再試験 問題一覧
次の問題(問102)へ