共通テスト(理科) 過去問
令和7年度(2025年度)追・再試験
問121 (化学(第5問) 問6)
問題文
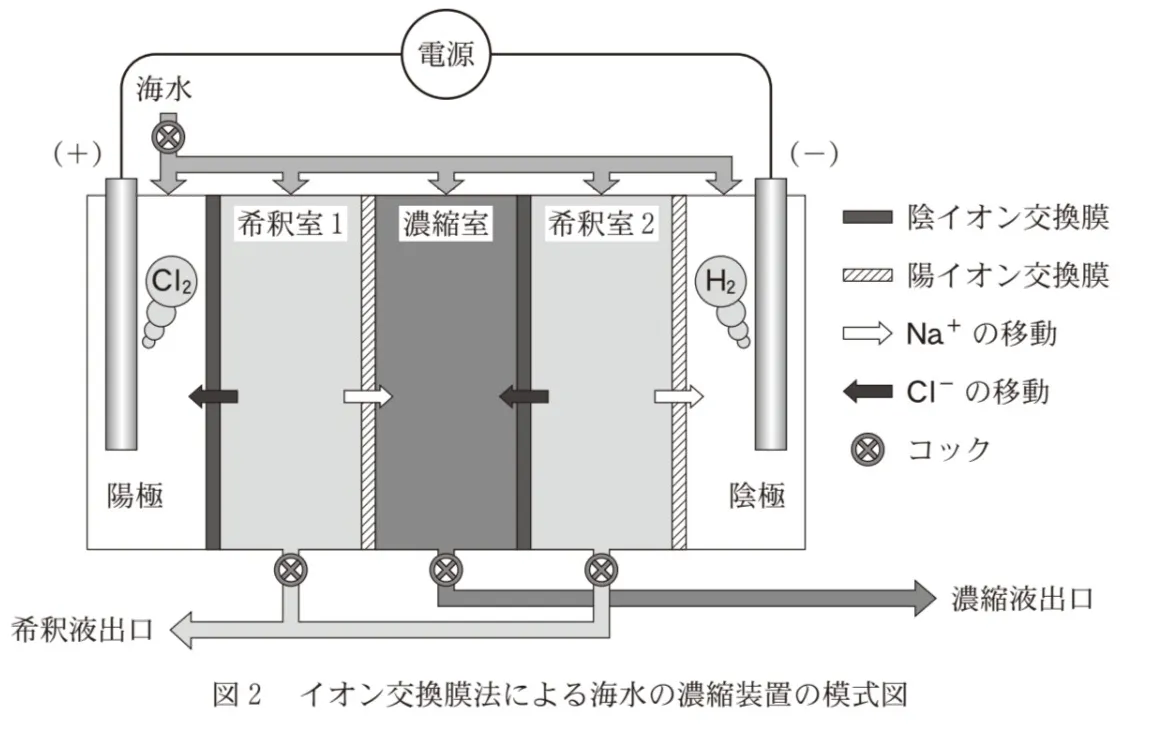
b 体積がそれぞれV(L)である希釈室1,濃縮室、希釈室2を、モル濃度がx(mol/L)であるNaCl水溶液で満たす。電流を流して濃縮室のNaClの物質量を希釈室1のNaClの物質量の2倍にするのに必要な電気量はいくらか。このときの電気量Q(C)を表す式として最も適当なものを、後の選択肢のうちから一つ選べ。ただし、NaCl水溶液中のNa+、Cl−以外のイオン、および溶液の体積変化は無視できるものとし、ファラデー定数をF(C/mol)とする。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和7年度(2025年度)追・再試験 問121(化学(第5問) 問6) (訂正依頼・報告はこちら)
b 体積がそれぞれV(L)である希釈室1,濃縮室、希釈室2を、モル濃度がx(mol/L)であるNaCl水溶液で満たす。電流を流して濃縮室のNaClの物質量を希釈室1のNaClの物質量の2倍にするのに必要な電気量はいくらか。このときの電気量Q(C)を表す式として最も適当なものを、後の選択肢のうちから一つ選べ。ただし、NaCl水溶液中のNa+、Cl−以外のイオン、および溶液の体積変化は無視できるものとし、ファラデー定数をF(C/mol)とする。

- xV/F
- xV/2F
- xV/3F
- xVF
- xVF/2
- xVF/3
正解!素晴らしいです
残念...

この過去問の解説 (1件)
01
陽極:2Cl-→Cl2+2e-・・・⑴
希釈室1から濃縮室へy(mol)移動したとすると、希釈室1と濃縮室のNaClの物質量はx(mol/L)✕V(L)=xV(mol)なので
(xV+y)mol:(xVーy)mol=2:1
これをyについて解くと、y=xV/3(mol)
式⑴より、希釈室1から濃縮室へ塩化物イオンCl-が2つ移動すれば2e-だけ電子も消費されたと考えることができるので、求める電気量は
xV/3(mol)✕F(C/mol)=xVF/3(C)
参考になった数0
この解説の修正を提案する
前の問題(問120)へ
令和7年度(2025年度)追・再試験 問題一覧
次の問題(問122)へ