共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問30 (化学基礎(第2問) 問1(1)
)
問題文
アボガドロは、気体の種類によらず、同温・同圧で同体積の気体には、同数の分子が含まれるという仮説を提唱した。この仮説は、今日ではアボガドロの法則として知られている。次の実験Ⅰは、アボガドロの法則に基づいて、貴ガス(希ガス)元素の一つであるクリプトンKrの原子量を求めることを目的としたものである。
実験Ⅰ
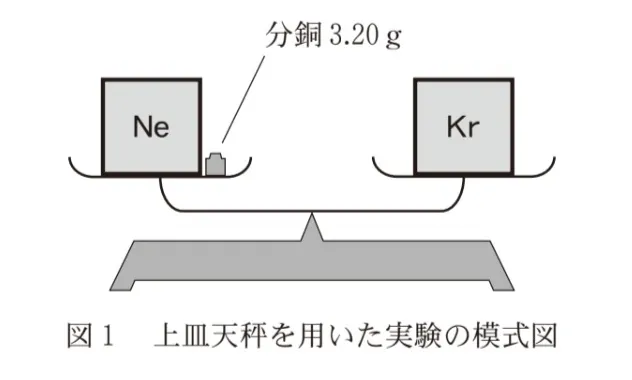
ネオンNe 1.00gが入った容器がある。大きさと質量が等しい別の容器に、同温・同圧で同じ体積のKrを入れ、両方の容器を上皿天秤(びん)にのせた。両方の皿がつり合うには、図1に示すように、Neが入った容器をのせた皿に3.20gの分銅が必要であった。
NeとKrの原子は、いずれも最外殻電子の数が( ア )個である。これらの原子は、他の原子と反応したり結合をつくったりしにくい。このため、価電子の数は( イ )個とみなされる。NeとKrはいずれも単原子分子として存在するので、Neの原子量が20であることを用いて、Krの原子量を求めることができる。
a 空欄( ア )に当てはまる数字として最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問30(化学基礎(第2問) 問1(1) ) (訂正依頼・報告はこちら)
アボガドロは、気体の種類によらず、同温・同圧で同体積の気体には、同数の分子が含まれるという仮説を提唱した。この仮説は、今日ではアボガドロの法則として知られている。次の実験Ⅰは、アボガドロの法則に基づいて、貴ガス(希ガス)元素の一つであるクリプトンKrの原子量を求めることを目的としたものである。
実験Ⅰ
ネオンNe 1.00gが入った容器がある。大きさと質量が等しい別の容器に、同温・同圧で同じ体積のKrを入れ、両方の容器を上皿天秤(びん)にのせた。両方の皿がつり合うには、図1に示すように、Neが入った容器をのせた皿に3.20gの分銅が必要であった。
NeとKrの原子は、いずれも最外殻電子の数が( ア )個である。これらの原子は、他の原子と反応したり結合をつくったりしにくい。このため、価電子の数は( イ )個とみなされる。NeとKrはいずれも単原子分子として存在するので、Neの原子量が20であることを用いて、Krの原子量を求めることができる。
a 空欄( ア )に当てはまる数字として最も適当なものを、次の選択肢のうちから一つ選べ。

- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 0
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
アボガドロの法則は問題に記載の通り、同温同圧で同体積の期待には同数の分子が含まれるというものです。具体的には、標準状態(0℃、1atm)にて、1molの気体分子は22.4Lを占めます。一緒に覚えておきたいこととして、アボガドロ数があり、これは物質量を定義します。1mol=6.02×1024個です。1ダース=12個の様な概念と考えるとわかりやすいでしょう。
貴ガスですが、最外殻電子が全て詰まった状態のため、反応性が低いと考えます。ちなみに、ヘネアルクリキセラドン(ヘリウム、ネオン、クリプトン、キセノン、ラドン)と覚えるとよいでしょう。
周期表2週目以降の最外殻電子は8個です。
参考になった数0
この解説の修正を提案する
02
この問題のポイントは貴ガスの性質を正しく理解できているかどうかにあります。
まず貴ガスについてですが、もともとは稀な気体であることから希ガスとも呼ばれています。
しかし空気中には、例えばアルゴンArは約0.93%含まれており、これは同じく空気中に含まれる二酸化炭素CO₂の約0.04%と比べて、かなり高い比率で含まれています。
こうしたことより、希ガスという名称はふさわしくないのではないか、という考え方が出てきました。
そこで、他の物質と反応しにくい「高貴な気体」という意味から、貴ガスともいわれるようになりました。
貴ガス原子の最外殻電子数はヘリウムHeが2個で、その他はすべて8個となります。
したがって空欄アに当てはまる数字として最も適当であるのは8ということが分かります。
参考になった数0
この解説の修正を提案する
03
ネオンおよびクリプトンは、希ガス元素です。
ヘリウムを除く、希ガス元素の最外殻電子の数は8個です。
ヘリウムを除く、希ガス元素の最外殻電子の数は8個であり、安定しています。このような電子配置をオクテットといいます。
参考になった数0
この解説の修正を提案する
前の問題(問29)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問31)へ