共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問95 (化学(第1問) 問4(a))
問題文
ある溶媒Aに溶解した安息香酸(分子式C7H6O2,分子量122)は、その一部が水素結合により会合して二量体を形成し、式(2)の化学平衡が成り立つ。
一方、溶媒Aに溶解したナフタレン(分子式C10H8,分子量128)は、カルボキシ基をもたないので、このような二量体を形成しない。
安息香酸による凝固点降下では、二量体は1個の溶質粒子としてふるまう。
そのため、ナフタレンによる凝固点降下と比較することで、二量体を形成する安息香酸の割合を知ることができる。
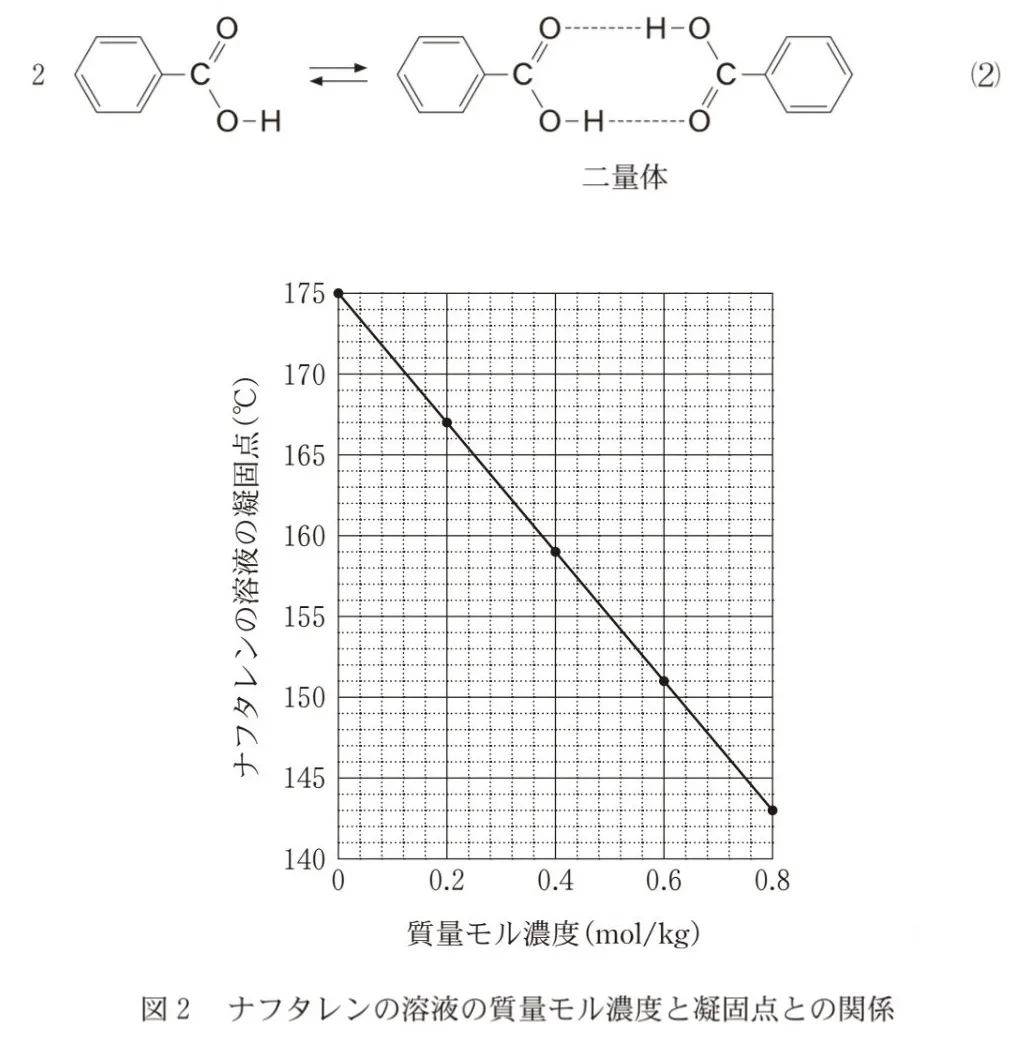
a 図2は、溶媒Aにナフタレンを溶解した溶液(ナフタレンの溶液)の質量モル濃度と凝固点との関係を表したグラフである。
図2から求められる溶媒Aのモル凝固点降下の値を2桁の整数で表すとき、空欄( )に当てはまる数字を、次の選択肢のうちから一つ選べ。
( )K・kg/mol
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問95(化学(第1問) 問4(a)) (訂正依頼・報告はこちら)
ある溶媒Aに溶解した安息香酸(分子式C7H6O2,分子量122)は、その一部が水素結合により会合して二量体を形成し、式(2)の化学平衡が成り立つ。
一方、溶媒Aに溶解したナフタレン(分子式C10H8,分子量128)は、カルボキシ基をもたないので、このような二量体を形成しない。
安息香酸による凝固点降下では、二量体は1個の溶質粒子としてふるまう。
そのため、ナフタレンによる凝固点降下と比較することで、二量体を形成する安息香酸の割合を知ることができる。
a 図2は、溶媒Aにナフタレンを溶解した溶液(ナフタレンの溶液)の質量モル濃度と凝固点との関係を表したグラフである。
図2から求められる溶媒Aのモル凝固点降下の値を2桁の整数で表すとき、空欄( )に当てはまる数字を、次の選択肢のうちから一つ選べ。
( )K・kg/mol

- 10
- 20
- 30
- 40
- 50
- 60
- 70
- 80
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
凝固点降下の公式
Δt=K·m
Δt:凝固点が下がった温度(K)
K: モル凝固点降下(K・kg/mol)
m: 質量モル濃度(mol/kg)
よって公式より
8=K×0.2
K=40
が答えとなります。
凝固点降下の公式は質量モル濃度を使うとしっかり覚えておきましょう。
参考になった数1
この解説の修正を提案する
02
モル凝固点降下の値は40K・kg/molとなります。
モル凝固点降下とはモル質量あたりの、
凝固する温度の低下値です。
つまり、モル凝固点降下は、図2のグラフの傾きに対応します。
(※グラフの傾きは負になりますが、低下を正としているので、
傾きの絶対値が凝固点降下の値になります。)
グラフの傾きを求めると(計算する2点はどこでもよい)、
8K /0.2(mol/kg)=40K・kg/mol
となり、
凝固点降下の値は40となります。
参考になった数0
この解説の修正を提案する
03
凝固点降下の公式を用いて解答します。
Δt=Kfm(Kf:モル凝固点降下)
非電解質の希薄溶液の凝固点降下度Δtは、溶質の種類に関係なく質量モル濃度m(mol/kg)に比例します。
図2より、0.80mol/kgのナフタレンの溶液の凝固点降下度は32Kであることが読み取れます。
よって、その数値を上式に代入すると
32K=Kf✕0.80mol/kg
となってKf=40K・kg/molとなることが分かります。
参考になった数0
この解説の修正を提案する
前の問題(問94)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問97)へ