共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問97 (化学(第1問) 問4(c))
問題文
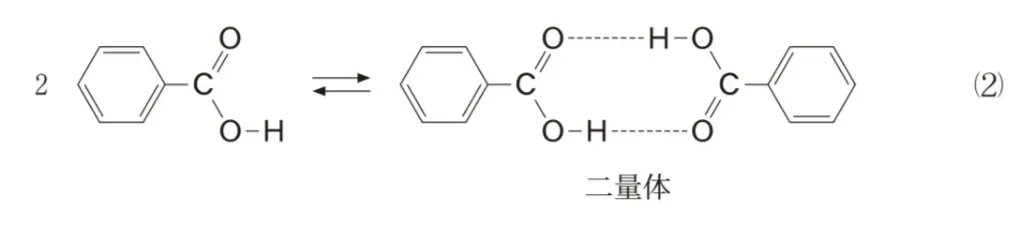
ある溶媒Aに溶解した安息香酸(分子式C7H6O2,分子量122)は、その一部が水素結合により会合して二量体を形成し、式(2)の化学平衡が成り立つ。
一方、溶媒Aに溶解したナフタレン(分子式C10H8,分子量128)は、カルボキシ基をもたないので、このような二量体を形成しない。
安息香酸による凝固点降下では、二量体は1個の溶質粒子としてふるまう。
そのため、ナフタレンによる凝固点降下と比較することで、二量体を形成する安息香酸の割合を知ることができる。
b 溶液中でどのくらいの安息香酸が二量体を形成しているかを示す値として、式(3)で定義される会合度βを求めたい。
β=二量体を形成している安息香酸の物質量/溶液に含まれる安息香酸の全物質量 (3)
ある質量モル濃度になるように溶媒Aに安息香酸を溶解し、この溶液(安息香酸の溶液)の凝固点を測定した。同じ質量モル濃度のナフタレンの溶液における凝固点降下度(凝固点降下の大きさ)ΔTfと安息香酸の溶液における凝固点降下度ΔTf′を比較したところ、ΔTf′=(3/4)ΔTfであった。このときのβの値として最も適当な数値を、次の選択肢のうちから一つ選べ。ただし、βの値は温度によらず変わらないものとする。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問97(化学(第1問) 問4(c)) (訂正依頼・報告はこちら)
ある溶媒Aに溶解した安息香酸(分子式C7H6O2,分子量122)は、その一部が水素結合により会合して二量体を形成し、式(2)の化学平衡が成り立つ。
一方、溶媒Aに溶解したナフタレン(分子式C10H8,分子量128)は、カルボキシ基をもたないので、このような二量体を形成しない。
安息香酸による凝固点降下では、二量体は1個の溶質粒子としてふるまう。
そのため、ナフタレンによる凝固点降下と比較することで、二量体を形成する安息香酸の割合を知ることができる。
b 溶液中でどのくらいの安息香酸が二量体を形成しているかを示す値として、式(3)で定義される会合度βを求めたい。
β=二量体を形成している安息香酸の物質量/溶液に含まれる安息香酸の全物質量 (3)
ある質量モル濃度になるように溶媒Aに安息香酸を溶解し、この溶液(安息香酸の溶液)の凝固点を測定した。同じ質量モル濃度のナフタレンの溶液における凝固点降下度(凝固点降下の大きさ)ΔTfと安息香酸の溶液における凝固点降下度ΔTf′を比較したところ、ΔTf′=(3/4)ΔTfであった。このときのβの値として最も適当な数値を、次の選択肢のうちから一つ選べ。ただし、βの値は温度によらず変わらないものとする。

- 0.13
- 0.25
- 0.50
- 0.75
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
答えはβ=0.5
となります。
いきなり計算を行う前にどうしてその現象が
発生したのか考えると理解が深まるでしょう。
凝固点降下度が下がった理由は、
安息香酸の一部が二量体化し、
溶質粒子数に基づく有効な質量モル濃度が下がったためです。
二量体化が起こると質量の総量は変わらず、
二量体は1個の溶質粒子としてふるまい、
溶質粒子として数えられる物質量が減少します。
モル凝固点降下は溶質の種類に関係なく、溶媒固有の値を取ります。
そのため、二量体を形成しないナフタレンを使用したときと、
一部が二量体化する安息香酸を使用したときの凝固点降下度を比較することで、
二量体を形成する安息香酸の割合を知ることができます。
上記のことを踏まえて、以下で式を立て計算を行います。
ナフタレンの溶液における凝固点降下度(凝固点降下の大きさ)ΔTfは以下の式で計算されます。
ΔTf=K×m
ΔTf:凝固点降下度(凝固点降下の大きさ)(K)
K: モル凝固点降下(K・kg/mol)
m: 質量モル濃度(mol/kg)
ここでは計算を簡単にするために、
K=40、m=10として計算を行いましょう。
会合度βという比を求める問題なので、Kとmは任意に設定して問題ないです。
設定した値を使って、ナフタレンによる凝固点降下度ΔTfを計算すると
ΔTf=K×m=40×10=400
となります。
安息香酸の溶液における凝固点降下度ΔTf′はΔTfを使って
ΔTf′=(3/4)ΔTf=(3/4)×400=300
となります。
この値は安息香酸の質量モル濃度m'を用いて以下の式で表されます。
ΔTf′=K×m'=40×m'=300・・・①
βを使って安息香酸の質量モル濃度m'を求めます。
この中には二量体になっているものと、なっていないものが
混ざっています。
それぞれ、βと1-βの割合で含まれています。
二量体は2分子で1粒子として振る舞うので
その物質量はβ/2として換算されます。
(例えば、全部で10molあるうち4molが二量体になっていると
4/2+6=8mol
として換算されます。
このときβ=0.4となります。)
そのため、βを用いて安息香酸の質量モル濃度m'を求めと
m'=10×{β/2+(1-β)}=10×(1-β/2)・・・②
となります。
β=0のとき、つまり二量体を形成している安息香酸が無いとき、
安息香酸の質量モル濃度m'はナフタレンの質量モル濃度と等しく、
m'=m=10
となります。
②を①に代入すると
40×10×(1-β/2)=300
400×(1-β/2)=300
1-β/2=3/4
β/2=1/4
β=1/2=0.5
となります。
※別解
直感的理解
凝固点降下が 3/4 になったということは
粒子数も 3/4 になったということを意味します。
つまり、
元10粒子 →3/4の 7.5粒子になったと考えられます。
式で表すと
10→10(1−β/2)
となるため、
1−β/2=3/4
β= 1/2
となります。
参考になった数0
この解説の修正を提案する
02
ここでは会合度という言葉を分かりやすく理解しておく必要があります。
会合度とは端的に表現すると会合する分子の割合です。
β=二量体を形成している安息香酸の物質量/溶液に含まれる安息香酸の全物質量
と定義されています。
割合を考える時には全体を1にすると式がシンプルになりますので、溶液に含まれる安息香酸の全物質量を1とします。
そうすると二量体を形成している安息香酸の物質量はβとなります。
二量体とは分子2個が重合して生成する物質なので、二量体はβ/2だけ生成します。
ここで二量体を形成していない安息香酸の物質量は(1ーβ)なので、分子全体の数としては
β/2+(1ーβ)=1ーβ/2
と表すことができます。
ΔTf'=3/4ΔTfより、1ーβ/2=3/4だから、これを計算するとβ=0.5となります。
参考になった数0
この解説の修正を提案する
03
溶液に含まれる安息香酸の全物質量を1とすると、
二量体を形成している安息香酸の物質量がβとなるので、
二量体はβ/2できることになります(二分子が会合するため)。
また二量体を形成していない安息香酸は1–βなので、
分子の数として数えると
β/2+(1–β)=1–β/2
となります。
これが0.75になれば良いので、
1–β/2=0.75
β=0.5
が答えとなります。
会合度という機器馴染みがない概念が出てきましたが、
落ち着いて全量を定義して考えてみましょう。
参考になった数0
この解説の修正を提案する
前の問題(問95)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問98)へ