共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問17 (化学基礎(第1問) 問2)
問題文
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
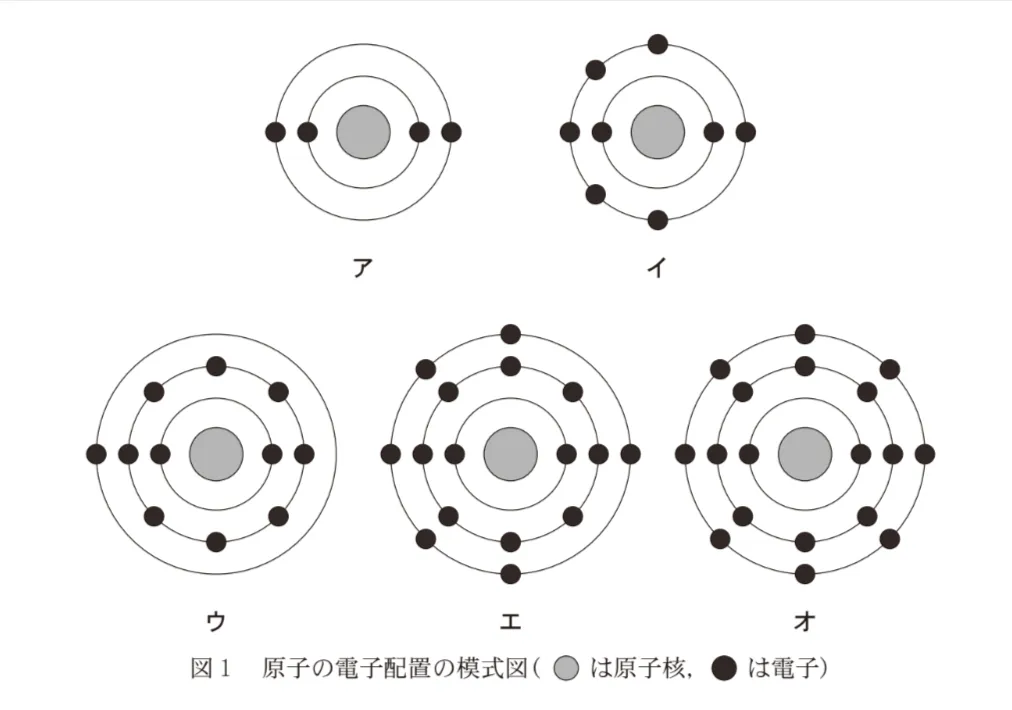
図1は、典型元素の原子ア~オの電子配置の模式図である。ア~オに関する記述として誤りを含むものはどれか。後の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問17(化学基礎(第1問) 問2) (訂正依頼・報告はこちら)
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
図1は、典型元素の原子ア~オの電子配置の模式図である。ア~オに関する記述として誤りを含むものはどれか。後の選択肢のうちから一つ選べ。

- アとイは第2周期の原子である。
- ウは1価の陽イオンになりやすい。
- イとエは同族元素の原子である。
- フッ化物イオンF-の電子配置は、オの電子配置と同じである。
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
原子番号 = 電子の数 であり、電子配置は内側から順にK、L、M、N殻となることを覚えておきましょう👍🏻
アとイは、どちらもL殻まで電子があります。すなわち、第2周期の原子です。
したがって、正解です。
最外殻( M殻)に電子が1個あります。最外殻電子が1個の原子は電子を放出するため、陽イオンになりやすいです。
したがって、正解です。
イとエは、最外殻電子の数が同じです。すなわち、同族元素の原子です。
したがって、正解です。
フッ素は9個の電子を持っています。すなわち、フッ化物イオンの電子は10個です。
したがって、不正解です。
参考になった数0
この解説の修正を提案する
02
問題にあるような図は電子配置図といわれ、原子核のまわりに電子殻が存在し
電子殻の中に電子が入っているように書き表します。
※厳密にはこのように均等な位置に電子は存在していません
電子の数=原子番号です。
アは電子が4つあるため、原子番号4のBeと考えられます。
イは電子が8つあるため、原子番号8のOと考えられます。
どちらも第2周期の原子です。
正しい文章です。
ウは最外殻に電子が1つあります。
この1つの電子を失うだけで1価の陽イオンになります(なりやすいです)。
正しい文章です。
ちなみにウは電子が11個あるため、原子番号11のNaと考えられます。
イとエはどちらも最外殻の電子が最大数-2です。
よってイとエは同族の原子です。
正しい文章です。
フッ素Fは原子番号9で電子を9つ持ちます。
フッ化物イオンF-は電子をさらに1つ多く持ちます。
よって電子を10個持ちます。
オの電子配置図には電子が18個あるため、F-の電子配置とは異なります。
誤った文章です。
参考になった数0
この解説の修正を提案する
前の問題(問16)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問18)へ