共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問88 (化学(第1問) 問6)
問題文
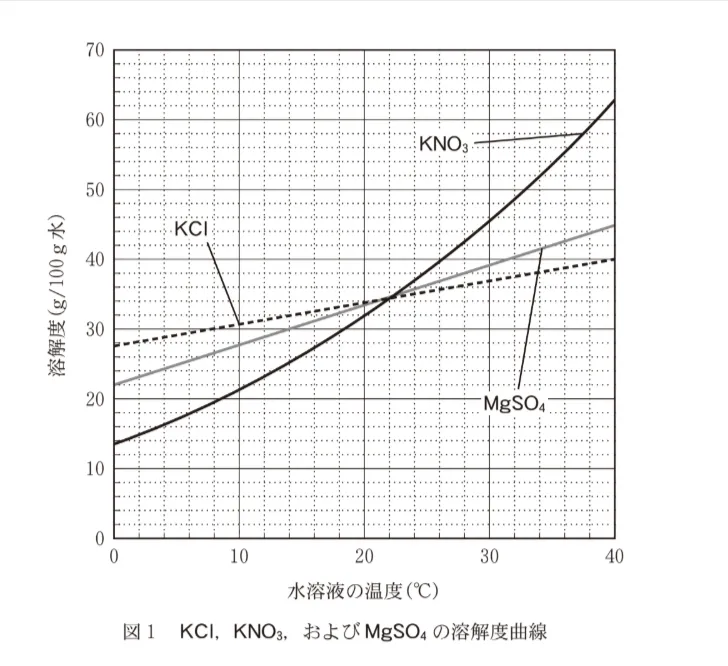
MgSO4の水溶液を冷却して得られる結晶は、MgSO4の水和物である。水100gに、ある量のMgSO4が溶けている水溶液Aを14℃に冷却する。このとき、析出するMgSO4の水和物の質量が12.3gであり、その中の水和水の質量が6.3gである場合、冷却前の水溶液Aに溶けているMgSO4の質量は何gか。最も適当な数値を、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問88(化学(第1問) 問6) (訂正依頼・報告はこちら)
MgSO4の水溶液を冷却して得られる結晶は、MgSO4の水和物である。水100gに、ある量のMgSO4が溶けている水溶液Aを14℃に冷却する。このとき、析出するMgSO4の水和物の質量が12.3gであり、その中の水和水の質量が6.3gである場合、冷却前の水溶液Aに溶けているMgSO4の質量は何gか。最も適当な数値を、次の選択肢のうちから一つ選べ。

- 28
- 30
- 32
- 34
- 36
- 42
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
水溶液Aを14℃に冷却した時に溶けているMgSO4の量をxgとします。
水溶液Aを14℃に冷却した時に溶媒として残っている水は
100gー6.3g=93.7g
となるので、MgSO4の溶解度は14℃で30g/100g水だから
xg:93.7g=30g:100g
これを解くとx=28.11g≒28.1gとなります。
析出したMgSO4の水和物が12.3gで、その中の水和水の質量が6.3gだから、この時のMgSO4の量は
12.3gー6.3g=6.0g
となります。
以上のことから、冷却前の水溶液Aに溶けているMgSO4の量は28.1g+6.0g=34.1gとなることが分かります。
参考になった数0
この解説の修正を提案する
02
溶解度と析出した水和物について計算する問題です。
14℃のMgSO4の溶解度は30 g/100g-水です。
14℃の時、水和物として6.3 gの水が析出されるので、溶媒として残っている水の量は、
100 - 6.3 = 93.7 gです。
ここに溶解度30 g/100g-水をかけると、14℃の水に溶解しているMgSO4の量が求められ、
30 X 93.7 =28.11 g
となります。
析出したMgSO4水和物のうち、MgSO4の質量は、
12.3-6.3 = 6.0 g
なので、
28.11 + 6.0 =34.11 ≒ 34 g
となります。
参考になった数0
この解説の修正を提案する
前の問題(問87)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問89)へ