共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問89 (化学(第2問) 問1)
問題文
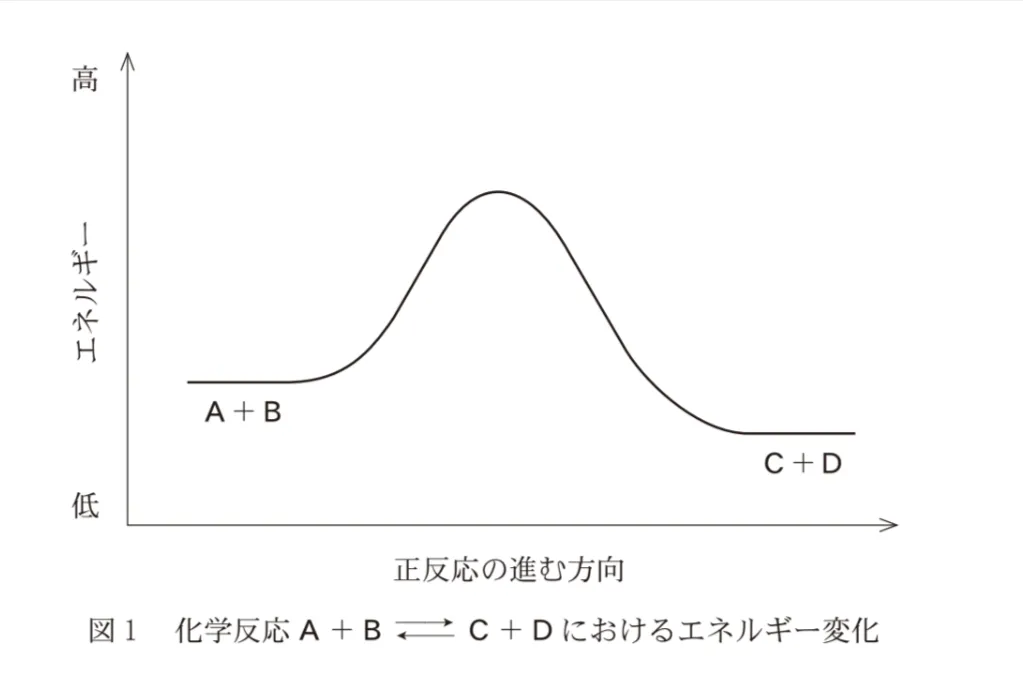
図は、化学反応A+B ⇄ C+Dにおけるエネルギー変化を表したものである。この化学反応のしくみに関する記述として下線部に誤りを含むものはどれか。最も適当なものを、後の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問89(化学(第2問) 問1) (訂正依頼・報告はこちら)
図は、化学反応A+B ⇄ C+Dにおけるエネルギー変化を表したものである。この化学反応のしくみに関する記述として下線部に誤りを含むものはどれか。最も適当なものを、後の選択肢のうちから一つ選べ。

- 反応物の濃度が大きくなると、反応に関与する粒子どうしの単位時間当たりの衝突回数が増える。
- 反応に関与する粒子どうしが衝突しても、活性化エネルギーを超えるエネルギーをもたないと反応が起こらない。
- 逆反応と正反応の活性化エネルギーの差が反応熱と等しくなるのは、同じ活性化状態(遷移状態)を経由して反応が進行するためである。
- 温度を上げると反応速度が大きくなるのは、活性化エネルギーが小さくなるためである。
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
化学反応速度に関する問題です。
正しい
反応物の濃度が大きくなると、反応速度も大きくなりますので、反応に関与する粒子どうしの単位時間当たりの衝突回数が増えます。
正しい
記述通りです。
正しい
記述通りです。
誤り
温度が上がると反応速度は大きくなりますが、活性化エネルギーの大きさに変化はありません。
参考になった数0
この解説の修正を提案する
02
化学反応のエネルギーについて問われている問題です。
正しいです。
正しいです。
正しいです。
誤りです。
温度を上げても活性化エネルギーは変化しません。
温度を上げると反応速度が大きくなるのは、活性化エネルギーよりも大きいエネルギーを持つ確率が上がるためです。
(参考)
反応速度k、活性化エネルギーE、温度Tの関係はアレニウスの式で表されます。
k = Aexp(-E/RT)
A,Rは定数
参考になった数0
この解説の修正を提案する
前の問題(問88)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問90)へ