共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問87 (化学(第1問) 問5)
問題文
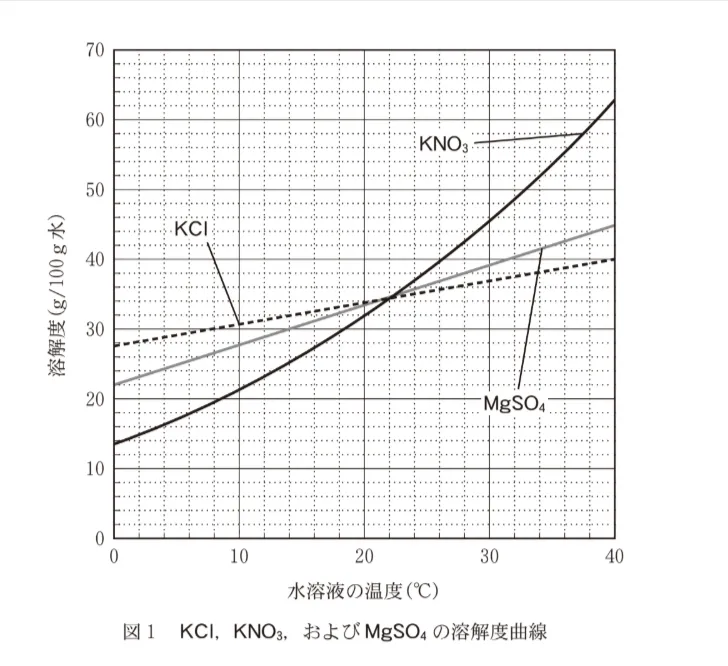
KCl(式量74.5)とKNO3(式量101)の水への溶解と水溶液からの析出に関する記述として誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問87(化学(第1問) 問5) (訂正依頼・報告はこちら)
KCl(式量74.5)とKNO3(式量101)の水への溶解と水溶液からの析出に関する記述として誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。

- KClの飽和水溶液とKNO3の飽和水溶液では、いずれも温度が低い方がカリウムイオンの濃度が小さい。
- 水100gにKClを溶かした30℃の飽和水溶液と、水100gにKNO3を溶かした30℃の飽和水溶液を調製し、両方の温度を10℃に下げると、析出する塩の質量はKClの方が大きい。
- 水100gにKClを溶かした22℃の飽和水溶液と、水100gにKNO3を溶かした22℃の飽和水溶液を比べると、カリウムイオンの物質量はKNO3の飽和水溶液の方が小さい。
- 水100gにKCl25gを加えると、10℃ではすべて溶けるが、水100gにKNO325gを加えると、10℃では一部が溶けずに残る。
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
溶解度曲線に関する問題です。
正しい
記述通りです。
KClとKNO3はいずれも温度が低い方が溶解度が小さいので、飽和水溶液ではいずれも温度が低い方がカリウムイオンの濃度が小さくなります。
誤り
KClとKNO3の溶解度曲線の傾きより、析出する塩の質量はKNO3の方が大きくなります。
正しい
分子量はKClよりKNO3の方が大きいので、同じ質量の溶解ならばKNO3の物質量の方が小さくなります。
正しい
溶解度曲線の10℃の時の溶解度から記述通りとなります。
参考になった数0
この解説の修正を提案する
02
溶解度曲線の読み方を問われている問題です。
正しいです。
溶解度曲線の傾きが正であれば、温度が低いほど、溶解度が下がります。
誤りです。
0~40℃の範囲でのKClとKNO3の溶解度の傾きを比較すると、
KNO3のほうが大きいです。
その為、KNO3のほうが温度変化で析出する量が大きいです。
正しいです。
22℃の溶解度はKClもKNO3も同程度です。
分子量はKCl<KNO3なので、同じ質量が溶解していれば、分子量の大きいKNO3の物質量のほうが小さくなります。
正しいです。
10℃の時の溶解度は、
KCl:約30 g/100g-水 > 25g/100g-水
KNO3:約21 g/100g-水 < 25g/100g-水
なので、KClはすべて溶けますが、KNO3は一部溶け残ります。
参考になった数0
この解説の修正を提案する
前の問題(問86)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問88)へ