共通テスト(理科) 過去問
令和6年度(2024年度)本試験
問24 (化学基礎(第1問) 問9)
問題文
下線を付した原子の酸化数を比べたとき、酸化数が最も大きいものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和6年度(2024年度)本試験 問24(化学基礎(第1問) 問9) (訂正依頼・報告はこちら)
下線を付した原子の酸化数を比べたとき、酸化数が最も大きいものを、次の選択肢のうちから一つ選べ。
正解!素晴らしいです
残念...

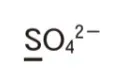


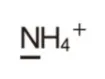
この過去問の解説 (3件)
01
酸化数に関する問題です。
まず、酸化数に関するルールについて確認していきます。
化合物中の水素原子の酸化数は原則として+1
化合物中の酸素原子の酸化数は原則として-2
単原子イオンの酸化数は、そのイオンの電荷に等しい
化合物全体を構成する原子の酸化数の総和は0になる
多原子イオンを構成する原子の酸化数の総和は、そのイオンの電荷に等しくなる
これらを踏まえて各選択肢を確認していきます。
酸化数の総和は-2より、Sはの酸化数は+6になります。
よってこの選択肢が正解となります。
酸化数の総和は0より、Nの酸化数は+5になります。
酸化数の総和は0より、Mnの酸化数は+4になります。
酸化数の総和は+1より、Nの酸化数は-3になります。
参考になった数0
この解説の修正を提案する
02
分子全体の酸化数の原理を覚えましょう。
1.SO42ー
分子全体の酸化数はー2となります。
Oの酸化数はー2なので、Sの酸化数は(ー2)ー(ー8)=+6です。
2.HNO3
分子全体の酸化数は0となります。
Hの酸化数は+1かつOの酸化数はー2なので、Nの酸化数は0ー(+1)ー(ー6)=+5です。
3.MnO2
分子全体の酸化数は0となります。
Oの酸化数はー2なので、Mnの酸化数は0ー(ー4)=+8です。
4.NH4+
分子全体の酸化数は+1です。
Hの酸化数は+1なので、Nの酸化数は(+1)ー(+4)=ー3です。
以上のことから酸化数が最も大きいのはSということが分かります。
参考になった数0
この解説の修正を提案する
03
酸化数の求め方を覚えておきましょう。
<基本ルール>
・単体:構成する原子の酸化数は0
・化合物(非イオン):分子全体の酸化数は0
・化合物(イオン):分子全体の酸化数=イオンの価数
・水素H:酸化数は+1
・酸素O:酸化数は-2
●SO42-
化合物(イオン)のため、分子全体の酸化数は-2です。
Oの酸化数が-2のため、O4の酸化数は-2×4=-8です。
残るSの酸化数は、-2-(-8)=+6です。
●HNO3
化合物(非イオン)のため、分子全体の酸化数は0です。
Hの酸化数が+1、O3の酸化数が-2×3=-6です。
残るNの酸化数は、0-(+1)-(-6)=+5です。
●MnO2
化合物(非イオン)のため、分子全体の酸化数は0です。
O2の酸化数が-2×2=-4です。
残るMnの酸化数は、0-(-4)=+4です。
●NH4+
化合物(イオン)のため、分子全体の酸化数は+1です。
H4の酸化数が+1×4=+4です。
残るNの酸化数は、+1-(+4)=-3です。
下線の原子のなかでもっとも酸化数が大きいのは、SO42-のS(酸化数+6)です。
参考になった数0
この解説の修正を提案する
前の問題(問23)へ
令和6年度(2024年度)本試験 問題一覧
次の問題(問25)へ