共通テスト(理科) 過去問
令和6年度(2024年度)本試験
問97 (化学(第2問) 問6)
問題文
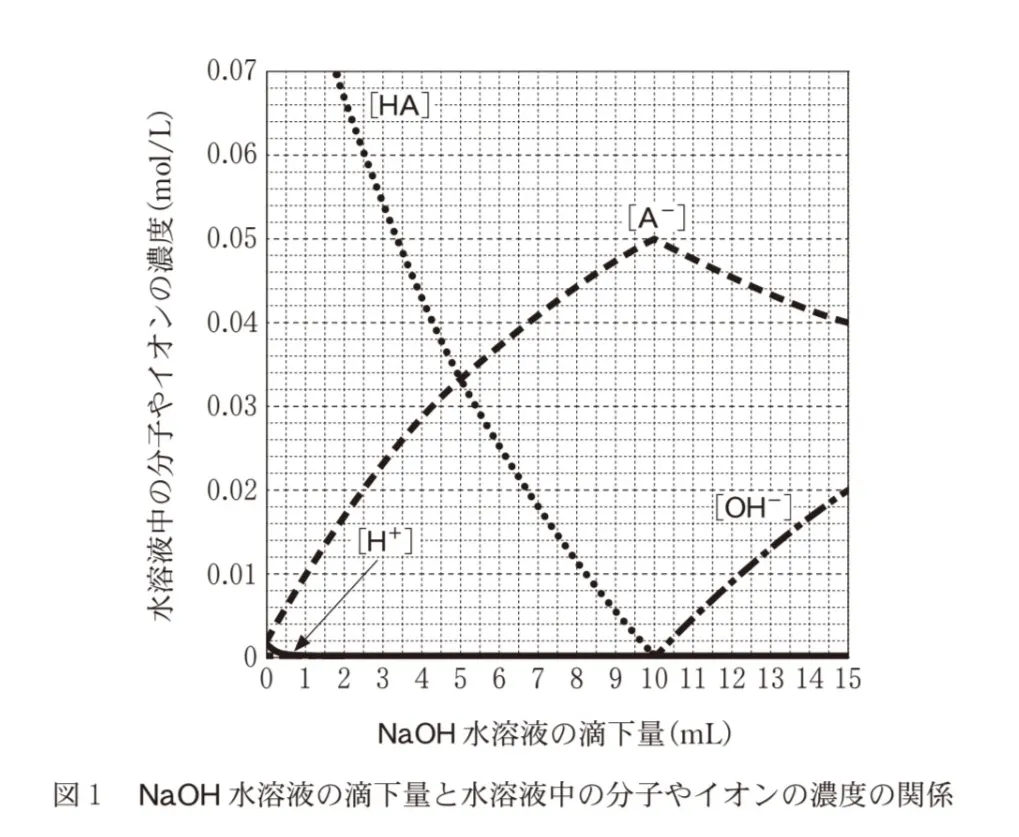
モル濃度0.10mol/LのHA水溶液10.0mLに、モル濃度0.10mol/LのNaOH水溶液を滴下すると、水溶液中のHA、H+、A−、OH−のモル濃度[HA]、[H+]、[A−]、[OH−]は、図1のように変化する。NaOH水溶液の滴下量が2.5mLのとき、H+のモル濃度は[H+]=8.1✕10−5mol/Lである。この条件において、NaOH水溶液の滴下に伴う水溶液中の分子やイオンの濃度変化を説明する記述として、下線部に誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和6年度(2024年度)本試験 問97(化学(第2問) 問6) (訂正依頼・報告はこちら)
モル濃度0.10mol/LのHA水溶液10.0mLに、モル濃度0.10mol/LのNaOH水溶液を滴下すると、水溶液中のHA、H+、A−、OH−のモル濃度[HA]、[H+]、[A−]、[OH−]は、図1のように変化する。NaOH水溶液の滴下量が2.5mLのとき、H+のモル濃度は[H+]=8.1✕10−5mol/Lである。この条件において、NaOH水溶液の滴下に伴う水溶液中の分子やイオンの濃度変化を説明する記述として、下線部に誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。

- NaOH水溶液の滴下量によらず、陽イオンの総数と陰イオンの総数は等しい。
- NaOH水溶液の滴下量によらず、[H+]と[OH−]の積は一定である。
- NaOH水溶液の滴下量が10mL未満の範囲では、HAの電離平衡の移動により[A−]が増加する。
- NaOH水溶液の滴下量が10mLより多い範囲では、中和反応により[A−]が減少する。
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
電気的中性条件、水のイオン積、電離平衡の知識を組み合わせて判断します。
正しい。
溶液は常に電気的中性条件を満たすため、陽イオンの総電荷と陰イオンの総電荷は常に等しくなります。
正しい。
温度一定のもとでは水のイオン積は常に一定です。
正しい。
NaOHを加えるとHAが中和されA-が生成します。さらにHAの電離平衡が右に移動することでも[A-]が増加します。
誤り=正解。
10mL以降はHAがほぼ全て中和済みのため中和反応はほぼ起きていません。[A-]が減少するのはNaOH水溶液の添加による希釈効果によるものです。
参考になった数0
この解説の修正を提案する
02
OH-のグラフに注目すると、NaOH水溶液(塩基)を10ml滴下したときに中和されることが分かります。
選択肢にも10mLが出ていることに注意して正誤の判断をします。
陽イオンの総数と陰イオンの総数は電気的な中和により打ち消しあうため等しくなります。
よってこの記述は正しいです。
[H+]と[OH−]の積は水溶液の温度変化がないことより一定となります。
よってこの記述は正しいです。
NaOH水溶液の滴下量が10mL未満の範囲では、
ルシャトリエの原理より[H+]が減少したときに、
HAの電離平衡の移動することより[A−]が増加します。
よってこの記述は正しいです。
NaOH水溶液の滴下量が10mLの時に中和されます。
なので中和反応により[A−]が減少することはありません。
この記述は誤り、よってこの選択肢が正解となります。
参考になった数0
この解説の修正を提案する
03
中和に関する問題です。今回の問題では、塩基を10ml滴下すると、中和されます。
電気的中和の関係から、水溶液中の陽イオンと陰イオンの総数は常に等しくなります。
水のイオン積は温度が等しい限り常に一定となり、25℃では1.0×10-14となります。
NaOHを滴下していくと、H+が中和され、減少していきます。その結果、ルシャトリエの原理より、H+を補うため、[HA]→[H+][A-]が進み、A-が増加していきます。
NaOHが10ml滴下された時点で中和は完了し、それ以降は中和は起こらず、NaOHが増えていくだけとなります。
参考になった数0
この解説の修正を提案する
前の問題(問96)へ
令和6年度(2024年度)本試験 問題一覧
次の問題(問98)へ