共通テスト(理科) 過去問
令和7年度(2025年度)本試験
問101 (化学(第2問) 問5)
問題文
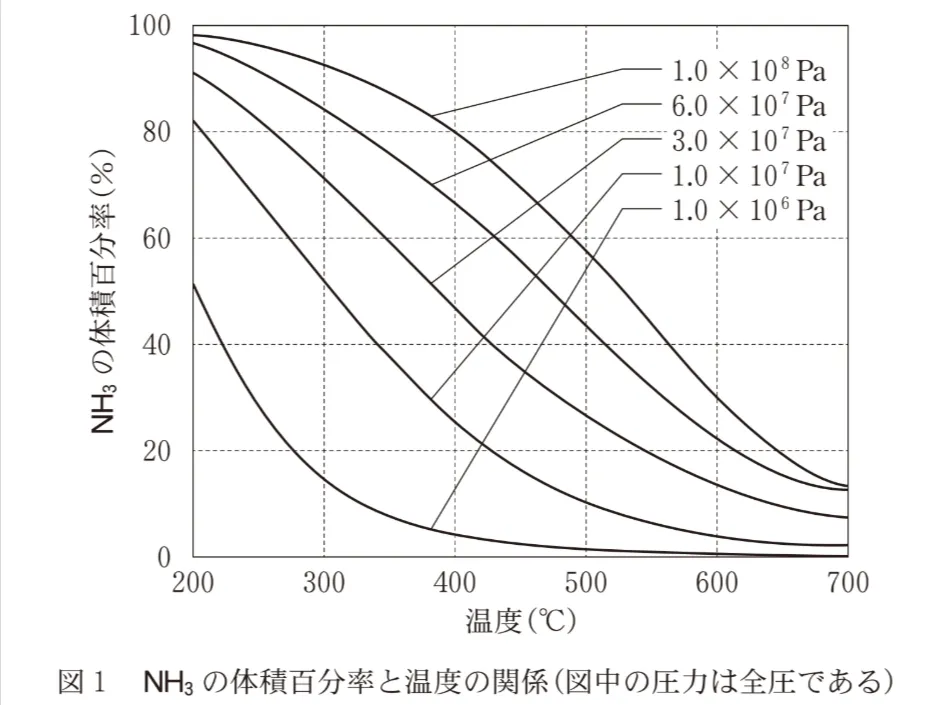
19世紀後半、肥料の原料であるアンモニアNH3の大量製造が必要となり、窒素N2と水素H2から直接NH3を得ることが化学者の課題であった。この課題は、ハーバー・ボッシュ法によって解決され、有用なNH3の合成方法となっている。この反応は、次の式(3)で表される。また、N2とH2を1:3の物質量の割合で反応させ、平衡状態に達したときのNH3の体積百分率と温度の関係を図1に示した。NH3の合成に関する後の問いに答えよ。
ただし、反応に用いる密閉容器中では、N2,H2とNH3は気体として存在するものとする。
N2+3H2 ⇄ 2NH3 ・・・(3)
密閉容器にN22.0molとH26.0molを入れ反応させたところ、平衡状態に達した。このとき、NH3は3.0mol生成し、全圧は1.0✕108Paであった。このときの反応温度は何℃であったか。最も適当な数値を、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和7年度(2025年度)本試験 問101(化学(第2問) 問5) (訂正依頼・報告はこちら)
19世紀後半、肥料の原料であるアンモニアNH3の大量製造が必要となり、窒素N2と水素H2から直接NH3を得ることが化学者の課題であった。この課題は、ハーバー・ボッシュ法によって解決され、有用なNH3の合成方法となっている。この反応は、次の式(3)で表される。また、N2とH2を1:3の物質量の割合で反応させ、平衡状態に達したときのNH3の体積百分率と温度の関係を図1に示した。NH3の合成に関する後の問いに答えよ。
ただし、反応に用いる密閉容器中では、N2,H2とNH3は気体として存在するものとする。
N2+3H2 ⇄ 2NH3 ・・・(3)
密閉容器にN22.0molとH26.0molを入れ反応させたところ、平衡状態に達した。このとき、NH3は3.0mol生成し、全圧は1.0✕108Paであった。このときの反応温度は何℃であったか。最も適当な数値を、次の選択肢のうちから一つ選べ。

- 350
- 420
- 490
- 560
- 650
正解!素晴らしいです
残念...

この過去問の解説 (1件)
01
平衡状態に達するまでに反応したN2をxmolとすると、平衡時のN2、H2及びNH3の物質量はそれぞれ(2.0ーx)mol、(6.0ーx)mol、2xmolとなります。
このときNH3は3.0mol生成したので
2xmol=3.0mol
これを解いてx=1.5mol
混合気体においては体積百分率と物質量の百分率は等しくなるので、平衡状態におけるNH3の体積百分率は、反応前の総物質量が8.0molだったから
2xmol/(8.0ー2x)mol✕100=2×1.5mol/(8.0ー2×1.5)mol✕100=60%
ここで補足説明すると、(8.0ー2x)molは平衡時における総物質量で、(2.0ーx)mol+(6.0ー3x)mol+2xmol=(8.0ー2x)molより求めることができます。
全圧は1.0×108Paであったので、グラフより反応温度は490℃となります。
参考になった数0
この解説の修正を提案する
前の問題(問100)へ
令和7年度(2025年度)本試験 問題一覧
次の問題(問102)へ