共通テスト(理科) 過去問
令和4年度(2022年度)本試験
問103 (化学(第3問) 問2)
問題文
必要があれば,原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ca 40
気体は、実在気体とことわりがない限り、理想気体として扱うものとする。
次の問いに答えよ。
ある金属元素Mが、その酸化物中でとる酸化数は一つである。この金属元素の単体Mと酸素O2から生成する金属酸化物MxOyの組成式を求めるために、次の実験を考えた。
実験
Mの物質量とO2の物質量の和を3.00✕10-2molに保ちながら、Mの物質量を0から3.00✕10-2molまで変化させ、それぞれにおいてMとO2を十分に反応させたのち、生成したMxOyの質量を測定する。
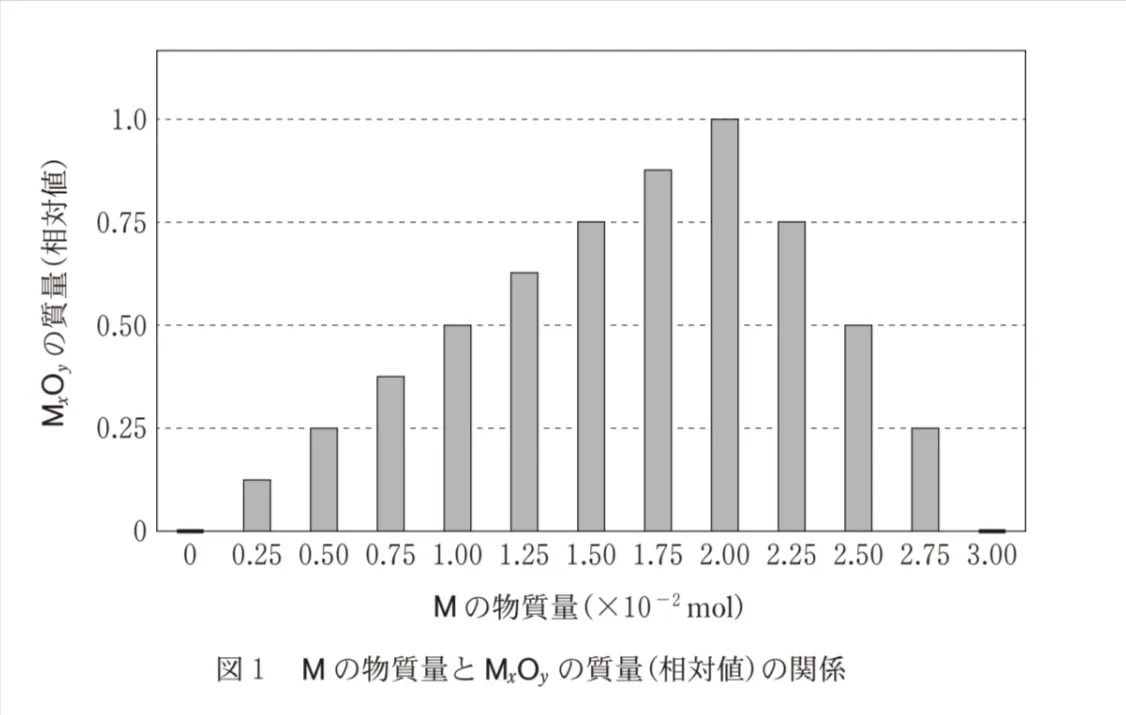
実験で生成するMxOyの質量は、用いるMの物質量によって変化する。図1は、生成するMxOyの質量について、その最大の測定値を1と表し、他の測定値を最大値に対する割合(相対値)として示している。図1の結果が得られるMxOyの組成式として最も適当なものを、後の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)本試験 問103(化学(第3問) 問2) (訂正依頼・報告はこちら)
必要があれば,原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ca 40
気体は、実在気体とことわりがない限り、理想気体として扱うものとする。
次の問いに答えよ。
ある金属元素Mが、その酸化物中でとる酸化数は一つである。この金属元素の単体Mと酸素O2から生成する金属酸化物MxOyの組成式を求めるために、次の実験を考えた。
実験
Mの物質量とO2の物質量の和を3.00✕10-2molに保ちながら、Mの物質量を0から3.00✕10-2molまで変化させ、それぞれにおいてMとO2を十分に反応させたのち、生成したMxOyの質量を測定する。
実験で生成するMxOyの質量は、用いるMの物質量によって変化する。図1は、生成するMxOyの質量について、その最大の測定値を1と表し、他の測定値を最大値に対する割合(相対値)として示している。図1の結果が得られるMxOyの組成式として最も適当なものを、後の選択肢のうちから一つ選べ。

- MO
- MO2
- M2O
- M2O3
- M2O5
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
MとO2を様々な割合で反応させています。
その割合によっては、どちらかの元素が余る場合も考えられますが
問題文に「MxOyの質量の最大値が1」と書かれています。
グラフを見ると、MxOyの質量が1となるのは、Mの物質量が2.00×10-2molの時です。
つまり、このときは過不足なく反応したと読み取ります。(難しいですね)
MとO2の物質量の和は3.00×10-2molのため
それぞれの物質量は、M:2.00×10-2mol、O2:1.00×10-2molになります。
M:O2=2:1のため、M:O=1:1です。
よって組成式はMOとなります。
参考になった数1
この解説の修正を提案する
02
グラフよりMxOyはMの物質量が2.00×10-2molのときに十分に反応していると考えられます。
このとき、O2の物質量は1.00×10-2molであるため、O原子の物質量は2.00×10-2mol。
よって組成式の比は1:1となります。
この選択肢が正解となります。
参考になった数0
この解説の修正を提案する
前の問題(問102)へ
令和4年度(2022年度)本試験 問題一覧
次の問題(問104)へ