共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問23 (化学基礎(第1問) 問4)
問題文
周期表の第2周期と第3周期の黒く塗りつぶした元素に関する記述として誤りを含むものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問23(化学基礎(第1問) 問4) (訂正依頼・報告はこちら)
周期表の第2周期と第3周期の黒く塗りつぶした元素に関する記述として誤りを含むものを、次の選択肢のうちから一つ選べ。
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
周期表の特徴について整理しましょう!
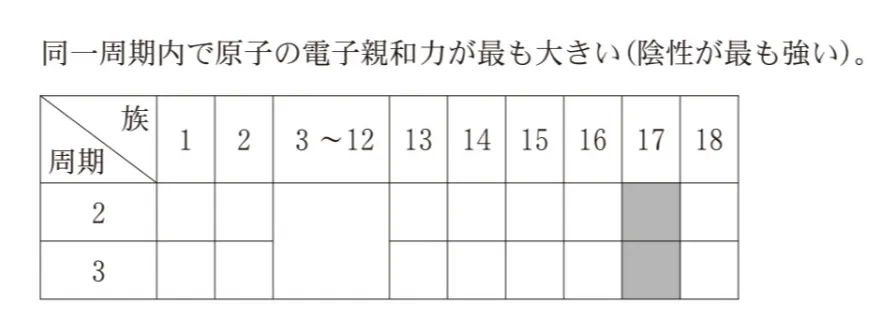
電子親和力とは、1価の陰イオンになるときに放出されるエネルギーのことです。
電子親和力は、周期表の右側に行くほど大きくなります。しかし、18族の希ガスは安定しているため、イオンになりません。つまり、17族が最も電子親和力が大きいです。
したがって、正解です。
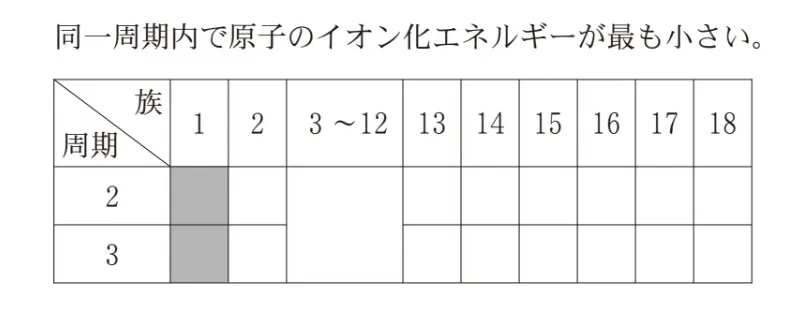
イオン化エネルギーとは、1価の陽イオンになるのに必要なエネルギーのことです。
イオン化エネルギーは、周期表の左下側に行くほど小さくなります。
したがって、正解です
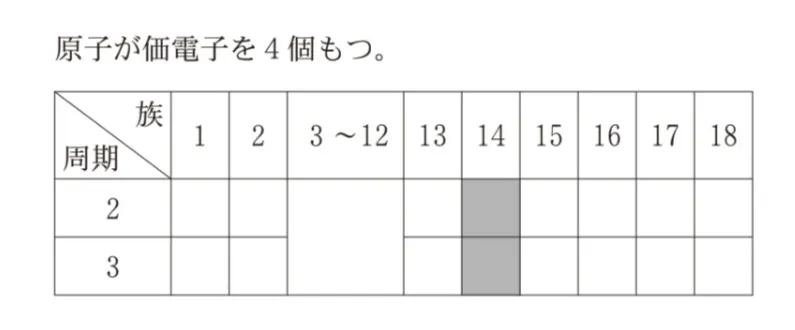
同じ族の元素は価電子数は等しいです。
14族元素の炭素の電子配置は
1s2,2s2,2p2
です。つまり、価電子は4個です。
したがって、正解です
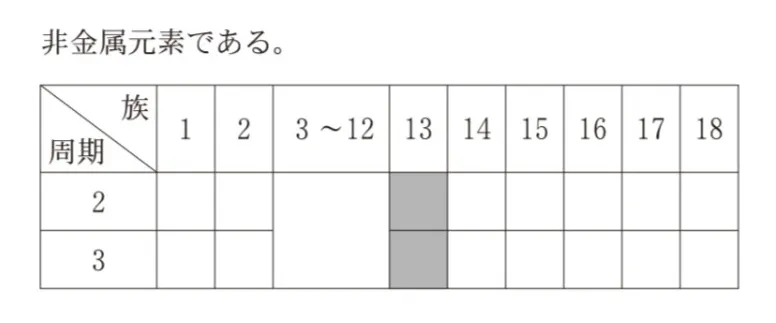
13族元素には金属、非金属どちらの元素もあります。
したがって、不正解です。
参考になった数0
この解説の修正を提案する
02
周期表とその規則性についての問題です。
金属・半金属・非金属の元素や、周期ごと・族ごとの規則性を理解しておきましょう。
正しい内容です。
同一周期内では右側に行くほど電子親和力が大きく
17族のハロゲンがその周期内では最大になります。
この傾向がみられるのは、周期表の右側に行くほど少しの電子を受け取るだけで
安定した電子配置(最外殻の電子が満たされ価電子数は0)になれるためです。
例えばFは電子を1つ受け取るだけで価電子0になります。
正しい内容です。
同一周期内では左側に行くほどイオン化エネルギーが小さいです。
左側に行くほど電子を少し失うだけで陽イオンになることができます。
簡単に陽イオンになる=イオン化に必要なエネルギーが小さい ということです。
Naは電子を1つ失うだけでNa+になります。
正しい内容です。
価電子とは、最外殻に存在する電子のことです。
第2周期14族元素は、最外殻L殻に電子が4つあり
第3周期14族元素は、最外殻M殻に電子が4つあります。
どちらも価電子を4つ持ちます。
誤った内容です。
13族元素は非金属と金属の両方があります。
非金属:ホウ素(B) ※厳密には金属と非金属の中間の性質をもつ半金属です
金属 :アルミニウム(Al)・ガリウム(Ga)・インジウム(In)
参考になった数0
この解説の修正を提案する
前の問題(問22)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問24)へ