共通テスト(理科) 過去問
令和5年度(2023年度)追・再試験
問21 (化学基礎(第1問) 問6)
問題文
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
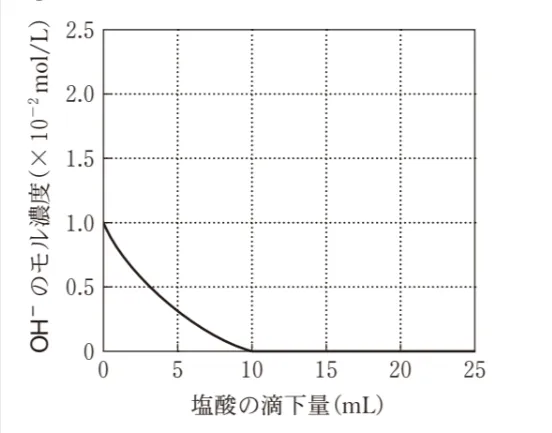
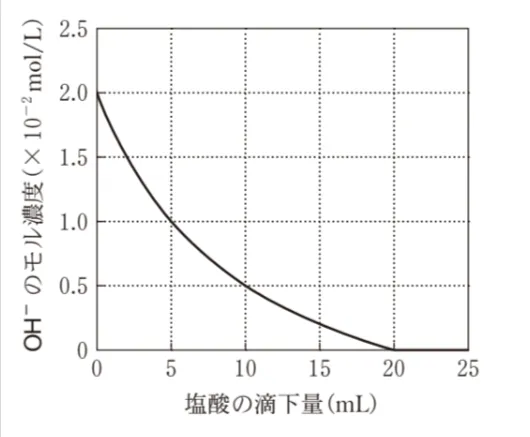
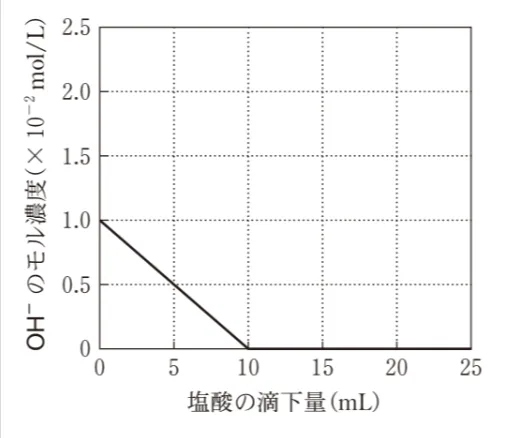
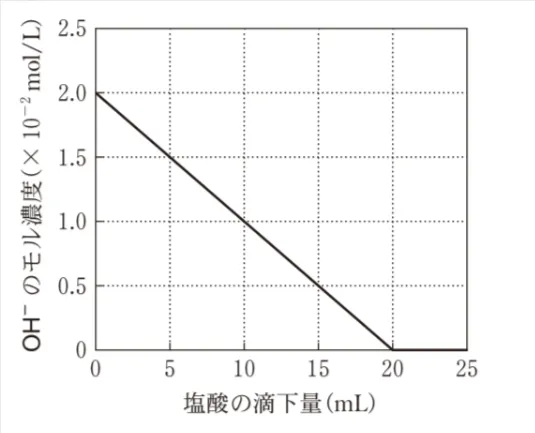
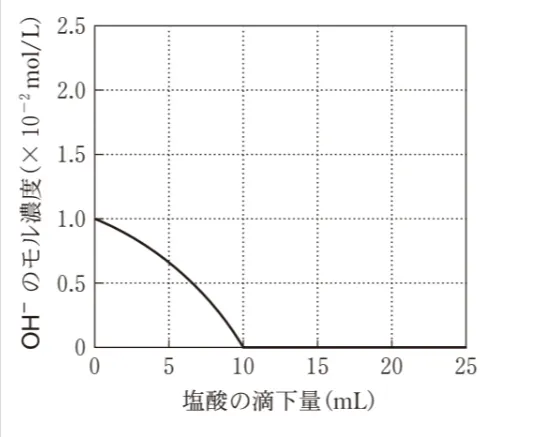
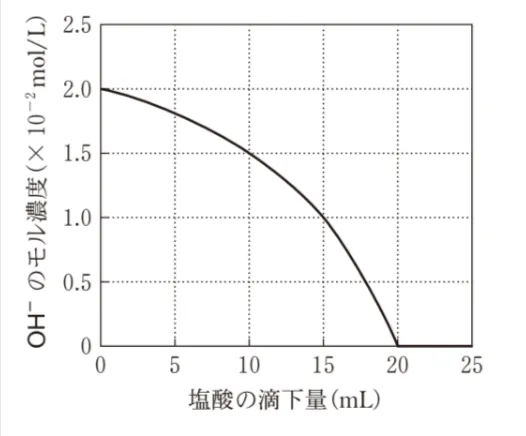
0.010mol/Lの水酸化カルシウムCa(OH)2水溶液10mLに0.010mol/Lの塩酸を滴下した。このときの水酸化物イオンOH-のモル濃度の変化を表すグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和5年度(2023年度)追・再試験 問21(化学基礎(第1問) 問6) (訂正依頼・報告はこちら)
H 1.0 C 12 O 16
Cl 35.5 K 39 Ca 40 Mn 55
次の問いに答えよ。
0.010mol/Lの水酸化カルシウムCa(OH)2水溶液10mLに0.010mol/Lの塩酸を滴下した。このときの水酸化物イオンOH-のモル濃度の変化を表すグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。
正解!素晴らしいです
残念...

この過去問の解説 (2件)
01
水酸化カルシウム Ca(OH)2 水溶液 : 0.010 mol/L、10 mL
塩酸 HCl: 0.010 mol/L、V mL
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Ca(OH)₂ の物質量は0.010 × 0.010 = 1.0×10-4 mol、OH-の物質量は1.0×10-4× 2 = 2.0×10-4 molです。
Ca(OH)2 1 mol が OH- 2 mol を出すので、OH-のモル濃度は0.010 × 2 = 2.0 × 10-2 mol/Lです。
また、加えた H⁺の物質量は0.010 × V/1000 = 1.0×10-⁵ × V molです。
このときの体積は(10+V)/1000 Lなので、
OH-のモル濃度が0になるときの塩酸の滴下量は以下のように求まります。
(2.0 × 10-4 - 1.0 × 10-⁵ × V)/{(10+V)/1000 L}
V = 20 mL
したがって、体積Vの増加に伴い、OH-のモル濃度が曲線的に小さくなり、塩酸20 mLにおいてOH-のモル濃度が0になります。
参考になった数0
この解説の修正を提案する
02
●塩酸滴下前のOH-のモル濃度
1molの水酸化カルシウムCa(OH)2から2molのOH-が電離します。
OH-のモル濃度は0.01mol/L×2=2.0×10-2mol/Lです。
塩酸の滴下量が0mlのときにOH-のモル濃度が2.0×10-2mol/Lの
グラフに選択肢が絞られます。
●塩酸10mlを滴下した時のOH-のモル濃度
・塩酸滴下前に存在したOH-の物質量
10ml/1000ml×0.02mol/L=2.0×10-4mol
・0.01mol/Lの塩酸10mlに含まれるH+の物質量
10/1000×0.01mol=1.0×10-4mol
・OH-とH+が反応して残るOH-の物質量
(2.0×10-4mol)-(1.0×10-4mol)=1.0×10-4mol
このとき液体は10ml+10ml=20mlあります(水酸化カルシウム+塩酸)
・残ったOH-のモル濃度
1000mlあたりに1000ml/20ml×1.0×10-4mol=0.5×10-2mol存在するため
塩酸を10ml滴下した時のOH-のモル濃度は0.5×10-2mol/Lとなります。
この条件にあてはまるグラフは1つに絞られます。
参考になった数0
この解説の修正を提案する
前の問題(問20)へ
令和5年度(2023年度)追・再試験 問題一覧
次の問題(問22)へ