共通テスト(理科) 過去問
令和6年度(2024年度)本試験
問26 (化学基礎(第2問) 問1)
問題文
必要があれば、原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Ar 40
宇宙ステーションの空気制御システムに関する次の文章を読み、後の問いに答えよ。
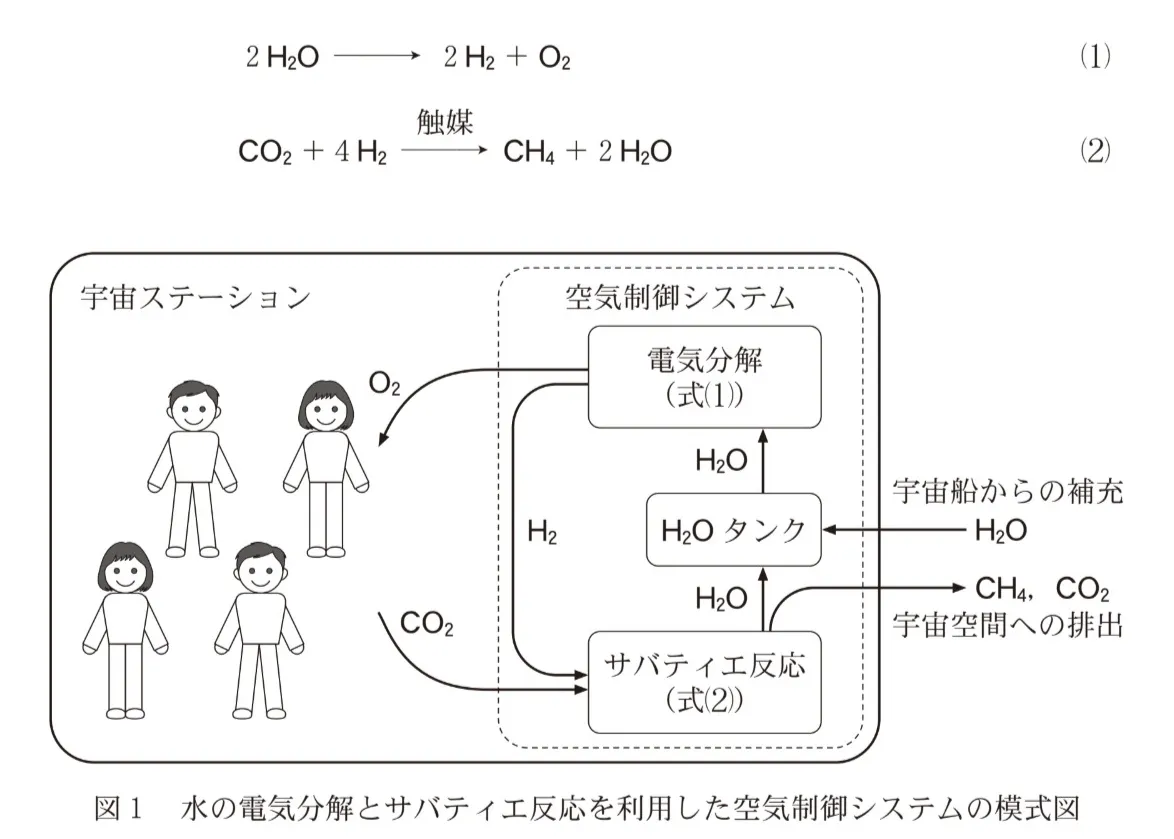
宇宙ステーションで人が生活するには、宇宙ステーション内の空気に含まれる酸素O2と二酸化炭素CO2の濃度を適切に管理する空気制御システムが必要である。空気制御システムでは、次の式(1)に示すように、水H2Oの電気分解を利用してO2が供給される。また、補充するH2Oの量を削減するために、式(2)のサバティエ反応の利用が試みられている(図1)。この反応では、触媒を用いてCO2と水素H2からメタンCH4とH2Oを生成するため、人の呼気に含まれるCO2の酸素原子をH2Oとして回収できる。
式(1)の電気分解に関する記述として誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和6年度(2024年度)本試験 問26(化学基礎(第2問) 問1) (訂正依頼・報告はこちら)
必要があれば、原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Ar 40
宇宙ステーションの空気制御システムに関する次の文章を読み、後の問いに答えよ。
宇宙ステーションで人が生活するには、宇宙ステーション内の空気に含まれる酸素O2と二酸化炭素CO2の濃度を適切に管理する空気制御システムが必要である。空気制御システムでは、次の式(1)に示すように、水H2Oの電気分解を利用してO2が供給される。また、補充するH2Oの量を削減するために、式(2)のサバティエ反応の利用が試みられている(図1)。この反応では、触媒を用いてCO2と水素H2からメタンCH4とH2Oを生成するため、人の呼気に含まれるCO2の酸素原子をH2Oとして回収できる。
式(1)の電気分解に関する記述として誤りを含むものはどれか。最も適当なものを、次の選択肢のうちから一つ選べ。

- 陽極側ではO2が発生する。
- 発生するO2は、水上置換法で捕集できる。
- 式(1)の反応は酸化還元反応である。
- 電気分解で発生するH2とO2の質量比は1:16となる。
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
電気分解に関する問題です。
水の電気分解では、陽極で電子を奪われる酸化反応が起こり酸素 が、陰極で電子を受け取る還元反応が起こり水素が発生します。
酸素は水に溶けにくい気体であるため、水上置換法で捕集することができます。
反応の前後で
H...+1→0
O...-2→0
と酸化数が変化しているのでこの反応は酸化還元反応です。
水の電気分解の化学反応式は
2H2O→2H2+O2
この式から、発生する水素と酸素のモル比は2:1であることがわかります。与えられた原子量を用いて、それぞれの質量を計算すると
水素...2×1.0×2=4.0g
酸素...1×16×2=32g
よって質量比は1:8となり、1:16は誤りとなるのでこの選択肢が正解となります。
参考になった数0
この解説の修正を提案する
02
電気分解に関する基礎的な問題です。
正しい
記述通りです。
陰極側では水素が発生します。
正しい
記述通りです。
O2は水に溶けにくいので水上置換法で捕集できます。
正しい
陽極では電子を放出し、陰極では電子を受け取っているので式⑴は酸化還元反応です。
誤り
式⑴よりH2のとO2の物質量の比は2:1です。
H2は2g/molでO2は32g/molですから、その質量比は
H2:O2=2g/mol✕2mol:32g/mol✕1mol=4g:32g=1g:8g
したがって質量比は1:8になります。
参考になった数0
この解説の修正を提案する
03
電気分解について理解を深めましょう💡
【陽極の反応】
4OH- → O2 + 2H2O +4e-
【陰極の反応】
2H2O + 2e- → H2 +2OH-
反応式より、陽極側からO2が発生することがわかります。
したがって、正解です。
O2は水に溶けにくいため、水上置換法で集めることができます。
したがって、正解です。
陰極で電子を受け取っているため還元反応、陽極で電子を放出しているため酸化反応しています。
したがって、正解です。
式(1)より、H2は2分子、O2は1分子であることがわかります。つまり、分子数の比はH2 : O2 = 2 mol : 1 molです。
H2のモル質量は2 g/mol、O2のモル質量は32 g/molなので、質量比は以下のように求まります。
H2 : O2 = 2 mol × 2 g/mol : 1 mol × 32 g/mol = 4 g : 32 g = 1 : 8
したがって、不正解です。
参考になった数0
この解説の修正を提案する
前の問題(問25)へ
令和6年度(2024年度)本試験 問題一覧
次の問題(問27)へ