共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問93 (化学(第1問) 問2)
問題文
実在気体は、理想気体の状態方程式に完全には従わない。
実在気体の理想気体からのずれを表す指標として、次の式(1)で表されるZが用いられる。
Z=PV/nRT (1)
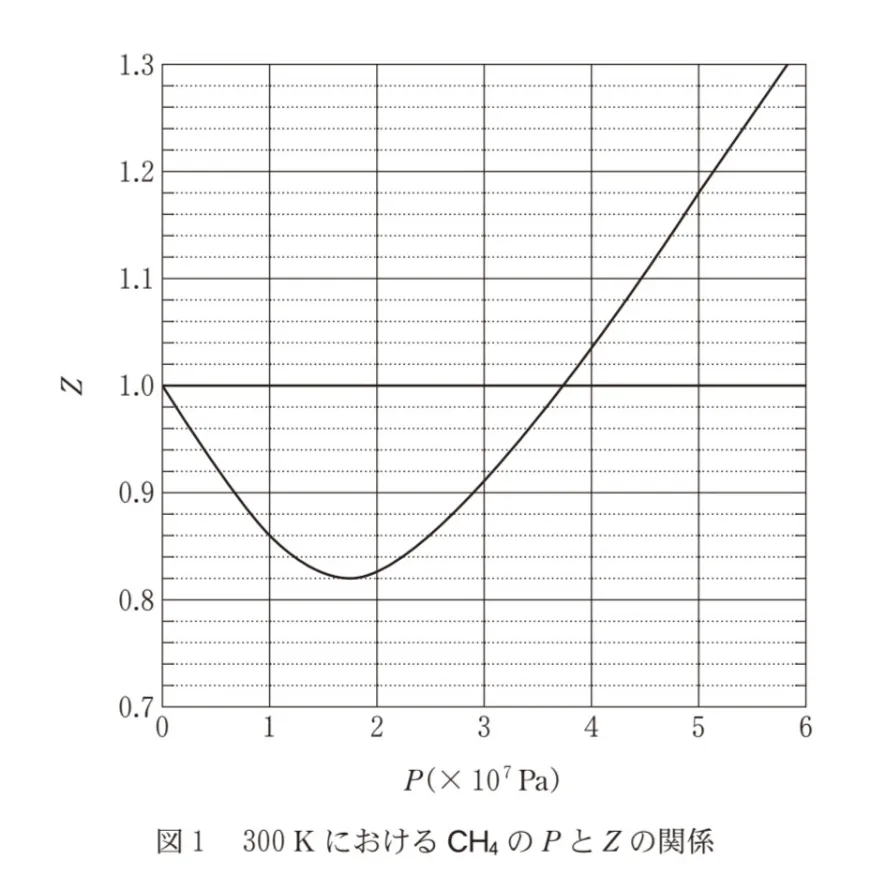
ここで、P,V,n,Tは、それぞれ気体の圧力、体積、物質量、絶対温度であり、Rは気体定数である。300KにおけるメタンCH4のPとZの関係を図1に示す。1molのCH4を300Kで1.0✕107Paから5.0✕107Paに加圧すると、Vは何倍になるか。最も適当な数値を、後の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問93(化学(第1問) 問2) (訂正依頼・報告はこちら)
実在気体は、理想気体の状態方程式に完全には従わない。
実在気体の理想気体からのずれを表す指標として、次の式(1)で表されるZが用いられる。
Z=PV/nRT (1)
ここで、P,V,n,Tは、それぞれ気体の圧力、体積、物質量、絶対温度であり、Rは気体定数である。300KにおけるメタンCH4のPとZの関係を図1に示す。1molのCH4を300Kで1.0✕107Paから5.0✕107Paに加圧すると、Vは何倍になるか。最も適当な数値を、後の選択肢のうちから一つ選べ。

- 0.15
- 0.20
- 0.27
- 0.73
- 1.4
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
方針は(1)式 Z=PV/nRT を変形した
V=ZnRT/P
に、加圧前の値と加圧後の値を
代入することで、
加圧前の体積V1と加圧後の体積V2を求めます。
その体積比V₂/V₁が求める値となります。
図1からCH4が1.0✕107PaのときのZと
5.0✕107PaのときのZを読み取ると、
1.0✕107Paのとき Z=0.86
5.0✕107Paのとき Z=1.18
です。
これらの値から体積を求めると、
V1=0.86/(1.0✕107)×1×R×300
V2=1.18/(5.0✕107)×1×R×300
となります。
(※圧力の(✕107)やnRTは加圧前後で変化せず
圧力比を求めるときに約分されるため、
この時点で省略しても問題ありません。)
したがって、体積比V₂/V₁は
V₂/V₁=1.18/(5.0×0.89)
となります。
分子分母両方を5で割り(2倍して小数点を左に1つずらす)、
V₂/V₁=1.18/(5.0×0.89)=0.23/0.86
となります。
この値は、0.23~0.3の
範囲になります。
(※0.23を1より小さい値で割っているため、
計算結果は0.23より大きくなります。
商が0.3だと割る数と商との積が0.24となるため、
0.3より小さいことが分かります。)
したがって、答えは
0.27となります。
参考になった数0
この解説の修正を提案する
02
この問題のポイントは与えられた式をVについて解き、図から正確な値を読み取れるかどうかにあります。
図1よりP=1.0×10⁷Paの時にZ=0.86、P=5.0×10⁷Paの時にZ=1.18になります。
式⑴をVについて解くと
V=ZnRT/P
となり、P=1.0×10⁷Paの時の体積をV₁、P=5.0×10⁷Paの時の体積をV₂とすると
V₁=0.86×1mol✕R✕300K/1.0×10⁷Pa
V₂=1.18×1mol✕R✕300K/5.0×10⁷Pa
と表すことができます。
このことから、V₂/V₁=0.274となり、最も適当な数値は0.27ということが分かります。
参考になった数0
この解説の修正を提案する
03
1.0✕107Paにおける1molのCH4で、温度が300Kのとき、
グラフからZ=0.86ですので、
Z=PV/nRTは
0.86=1.0✕107×V/(1✕R✕300)
となり、
V=2.58✕10–5✕Rとなります。
一方で、5.0✕107Paに加圧したとき、
グラフからZ=1.18ですので、
Z=PV/nRTは
1.18=5.0✕107×V/(1✕R✕300)
となり、
V=7.08✕10–6✕Rとなります。
よって、
(7.08✕10–6✕R)/(2.58✕10–5✕R)=0.274・・・=0.27
が答えとなります。
知らない式が出てきた場合でも、わかる数字を代入してみましょう。
知らない式だからこそ誰でも解けるように問題文にすべて情報が載っているはずです。
参考になった数0
この解説の修正を提案する
前の問題(問92)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問94)へ