共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問103 (化学(第2問) 問4(b))
問題文
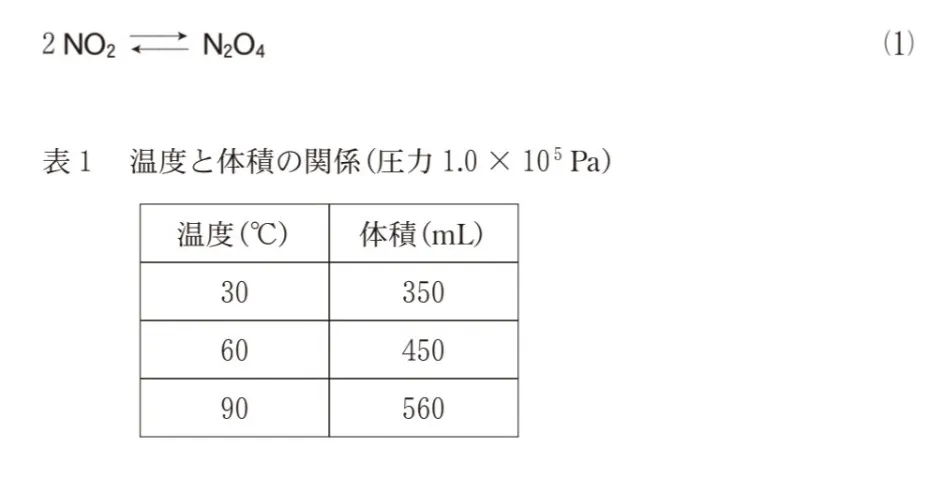
ピストンの付いた密閉容器に2.0✕10-2molのNO2を入れ、圧力1.0✕105Paのもとで温度を変えて平衡に達したときの体積を測定した。30℃、60℃、90℃での測定結果を表1に示す。表1から、温度が上昇すると平衡が( ア )に移動したことがわかる。
また、NO2からN2O4が生成する反応(式(1)の正反応)は、( イ )反応であることがわかる。後の問いに答えよ。
ただし、気体定数はR=8.3✕103Pa・L/(K・mol)とする。
b 温度60℃では、初期のNO2の物質量2.0✕10-2molの何%がN2O4に変化しているか。最も適当な数値を、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問103(化学(第2問) 問4(b)) (訂正依頼・報告はこちら)
ピストンの付いた密閉容器に2.0✕10-2molのNO2を入れ、圧力1.0✕105Paのもとで温度を変えて平衡に達したときの体積を測定した。30℃、60℃、90℃での測定結果を表1に示す。表1から、温度が上昇すると平衡が( ア )に移動したことがわかる。
また、NO2からN2O4が生成する反応(式(1)の正反応)は、( イ )反応であることがわかる。後の問いに答えよ。
ただし、気体定数はR=8.3✕103Pa・L/(K・mol)とする。
b 温度60℃では、初期のNO2の物質量2.0✕10-2molの何%がN2O4に変化しているか。最も適当な数値を、次の選択肢のうちから一つ選べ。

- 1.9
- 3.7
- 8.1
- 19
- 37
- 81
正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
気圧や気体定数が示されていることから状態方程式を
用いる問題だと考えられます。
表1と問題文から状態方程式に代入する値を読み取ります。
平衡状態時の物質量をN[mol]とします。
この物質量は
NO2の物質量n1と
N2O2の物質量n2の和です。
N=n1+n2・・・①
状態方程式は
1.0×105Pa✕450/1000L=Nmol✕8.3×103Pa・L/K・mol✕333K
となり、
物質量Nは
N=(1.0×105Pa✕450/1000L)/(8.3×103Pa・L/K・mol✕333K)
=(0.45×105)/(8.3×103✕333)[mol]
=0.01628[mol]・・・②
となります。
初期のNO2の物質量2.0✕10-2mol中の
N2O4に変化している割合をx(100x%)とする。
xを用いてNO2の物質量n1とN2O2の物質量n2を
表すと、
n1=2.0✕10-2×(1-x)mol
n2=2.0✕10-2×x×1/2mol
となります。
(1)の化学平衡から
NO2とN2O2の生成割合は
2:1になるため、
n2では最後に1/2をかけています。
①にそれぞれ代入して
N=n1+n2=2.0✕10-2×(1-x)+2.0✕10-2×x×1/2
=2.0✕10-2×[(1-x)+x/2]
=2.0✕10-2×[1-(x/2)]
=0.02-0.0x
となります。
②の値と比較して
0.01628=0.02-0.0x
0.0x=0.00372
x=0.372
となります。
よって、
0.372=37%
が答えとなります。
参考になった数0
この解説の修正を提案する
02
平衡状態におけるN2O4の物質量をXmolとしたときの全物質量の求め方ですが、平衡時のN2O4の物質量をXmolとしているので、2NO2の物質量は(2.0×10-2ー2X)molとなります。
よって全物質量は(2.0×10-2ー2X)+X=(2.0×10-2ーX)molと考えることができます。
また気体の状態方程式より
1.0×105Pa✕450/1000L=(2.0×10-2ーX)mol✕8.3×103Pa・L/K・mol✕333K
これをXについて解くと、X=3.72×10-3mol
最初にあったNO2は2.0×10-2molで、N2O4がXmolできると、そのとき使われたNO2は2Xmolです。したがって割合は
2X/2.0×10-2×100
=2×3.72×10-3/2.0×10-2×100
=37.2%
となります。
よって最も適当な数値は37ということが分かります。
参考になった数0
この解説の修正を提案する
03
初期のNO2の物質量2.0✕10-2molは、温度60℃,圧力1.0✕105Paでは
PV=nRTより、
V=2.0✕10-2mol ✕ 8.3✕103Pa・L/(K・mol)✕ 333 K / 1.0✕105 Pa
=0.55 L
の体積を持ちます。
このうちx%がN2O4に変化しているとすると、
NO2が0.55✕(1-x/100) L
N2O4が0.55✕(x/100)/2 L
の体積となるので、
0.55✕(1-x/100) + 0.55✕(x/100)/2 = 0.45
x=400/11=37(有効数字2桁)
気体の状態方程式から体積をきちんと求めましょう。
また反応によって体積がどのように変化するか、きちんと理解しましょう。
参考になった数0
この解説の修正を提案する
前の問題(問102)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問104)へ