共通テスト(理科) 過去問
令和4年度(2022年度)追・再試験
問123 (化学(第5問) 問2)
問題文
必要があれば、原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Mg 24 Cl 35.5 Cu 64 Zn 65 Ag 108
気体は、実在気体とことわりがない限り、理想気体として扱うものとする。
次の文章を読み、後の問いに答えよ。
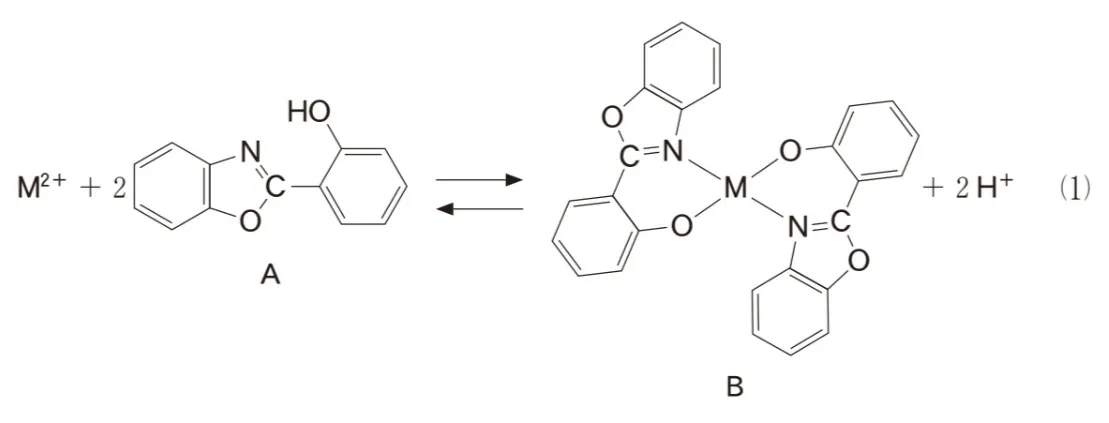
水溶液中に少量含まれる金属イオンの物質量を求めたいとき、分子量の大きい有機化合物を金属イオンに結合させて生成する沈殿の質量をはかる方法がある。この有機化合物の例として、化合物A(分子式C13H9NO2,分子量211)がある。pHを適切に調整すると、式(1)のように化合物Aの窒素原子と酸素原子が価の金属イオンM2+に配位結合し、M2+が化合物Bとしてほぼ完全に沈殿する。
式(1)のM2+としてCu2+を用いて次の実験を行った。0molから0.005moLまでのCu2+を含む水溶液を用意し、それぞれの水溶液に0.0040molの化合物Aを加え、pHを調整してCu2+と十分に反応させ、化合物Bを沈殿させた。
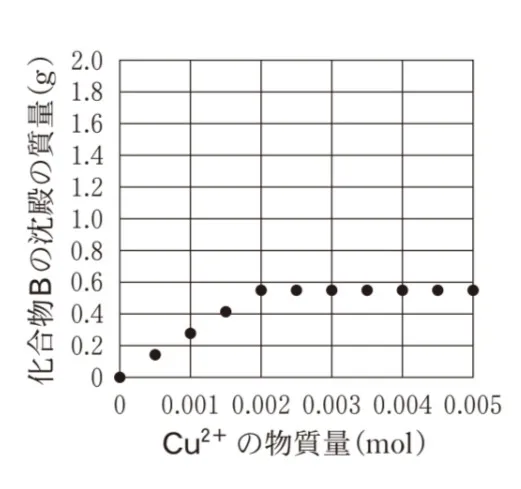
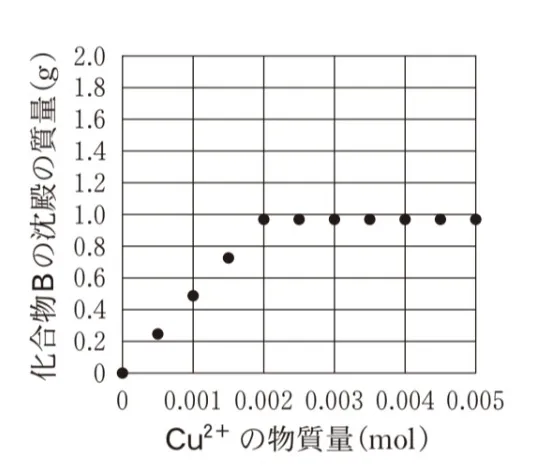
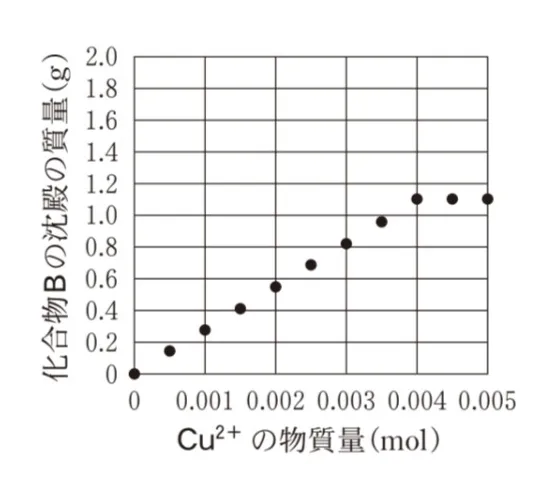
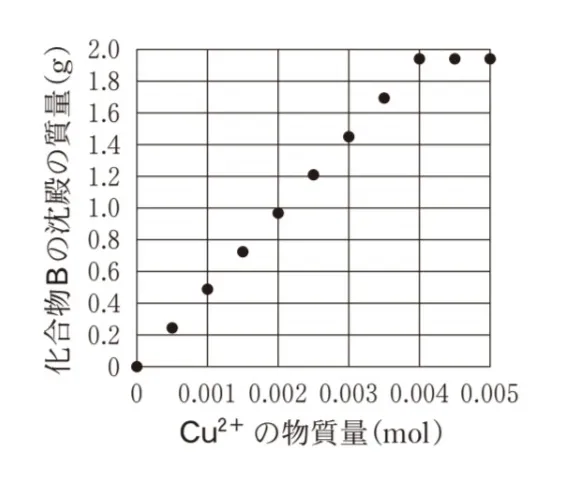
用意した水溶液中のCu2+の物質量と、生じた化合物Bの沈殿の質量の関係を表したグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。
このページは閲覧用ページです。
履歴を残すには、 「新しく出題する(ここをクリック)」 をご利用ください。
問題
共通テスト(理科)試験 令和4年度(2022年度)追・再試験 問123(化学(第5問) 問2) (訂正依頼・報告はこちら)
必要があれば、原子量は次の値を使うこと。
H 1.0 C 12 N 14 O 16 Mg 24 Cl 35.5 Cu 64 Zn 65 Ag 108
気体は、実在気体とことわりがない限り、理想気体として扱うものとする。
次の文章を読み、後の問いに答えよ。
水溶液中に少量含まれる金属イオンの物質量を求めたいとき、分子量の大きい有機化合物を金属イオンに結合させて生成する沈殿の質量をはかる方法がある。この有機化合物の例として、化合物A(分子式C13H9NO2,分子量211)がある。pHを適切に調整すると、式(1)のように化合物Aの窒素原子と酸素原子が価の金属イオンM2+に配位結合し、M2+が化合物Bとしてほぼ完全に沈殿する。
式(1)のM2+としてCu2+を用いて次の実験を行った。0molから0.005moLまでのCu2+を含む水溶液を用意し、それぞれの水溶液に0.0040molの化合物Aを加え、pHを調整してCu2+と十分に反応させ、化合物Bを沈殿させた。
用意した水溶液中のCu2+の物質量と、生じた化合物Bの沈殿の質量の関係を表したグラフとして最も適当なものを、次の選択肢のうちから一つ選べ。

正解!素晴らしいです
残念...

この過去問の解説 (3件)
01
(1)からM2+1molに対して(この問題ではCu2+)化合物Aは2mol 反応し、
1molの化合物Bと2molのH+を生じる。
よって、0.0040molの化合物Aをと完全に反応するCu2+は
0.0020molです。
そしてこの反応で0.0020molの化合物Bが生成されます。
化合物Bの分子量を求めます。
化合物Bは1molのCu2+と2molの 化合物Aが結合し、
2molのH+が取れています。
よって、化合物Bの分子量は
Cuの原子量+(化合物Aの分子量)×2-(水素原子の原子量)×2
64+211×2-2=484
となります。
0.0020molの化合物Bの重さは、
0.0020×484=0.968 g
となり、
適切なグラフはCu2+の物質量が0.002molで傾きが変わり、
生じた化合物Bの沈殿の質量の値が0.968 gで横ばいになる②のグラフです。
参考になった数0
この解説の修正を提案する
02
式⑴より0.0040molの化合物Aと反応できるのは0.0020molのCu2+となります。
よってCu2+が0.0020molで飽和しています。
またCu2+0.0020molに対して、沈殿Bは0.0020mol生成するので、その質量は化合物Bの分子量が484だから
0.0020mol✕484g/mol=0.968g
となります。
つまり、この2つの条件を満たすグラフを選べばよいということが分かります。
参考になった数0
この解説の修正を提案する
03
0.0040molの化合物Aと反応できるCu2+は0.0020molなので、
0.0020molで飽和しているものを選びます。
またCu2+0.0020molに対して、沈澱Bは0.0020molできるので、
0.0020×483.5=0.967 g
で飽和しているものを選びます。
参考になった数0
この解説の修正を提案する
前の問題(問121)へ
令和4年度(2022年度)追・再試験 問題一覧
次の問題(問124)へ